1. 领域背景与文献
文献英文标题:Long non-coding RNA SOX2OT in tamoxifen-resistant breast cancer;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:肿瘤学(乳腺癌内分泌治疗耐药)。
激素受体阳性乳腺癌是乳腺癌最常见的亚型,占所有乳腺癌病例的60%~70%,内分泌治疗是该亚型的核心治疗方案,其中他莫昔芬作为选择性雌激素受体调节剂,已在临床应用数十年,可显著降低早期患者的复发和死亡风险。领域共识:约30%的激素受体阳性乳腺癌患者在接受他莫昔芬治疗过程中会出现获得性耐药,耐药后的肿瘤侵袭性增强,治疗难度大幅提升,是目前HR阳性乳腺癌临床管理的核心难题。近年来长非编码RNA(lncRNA)的表观遗传调控作用成为肿瘤耐药研究的热点,已有研究证实多个lncRNA可通过调控ER信号通路、旁路激活等机制参与他莫昔芬耐药的发生,但目前lncRNA SOX2OT在该耐药亚型中的功能和调控机制尚未明确,且其与已知干性相关因子SOX2的交互作用、与肿瘤微环境的潜在关联均缺乏研究支持。本研究针对这一研究空白,旨在明确SOX2OT在他莫昔芬耐药乳腺癌中的表达特征与生物学功能,为内分泌耐药的机制解析和新型标志物开发提供实验依据。
2. 文献综述解析
作者的文献综述按照研究主题维度分为三个模块展开,分别为HR阳性乳腺癌内分泌治疗耐药的临床与基础研究进展、lncRNA在肿瘤进展与耐药中的功能研究、SOX2OT的现有研究基础,系统梳理了领域内的现有进展与未解决问题。
现有研究支持HR阳性乳腺癌内分泌治疗的生存获益显著,但耐药问题始终是限制患者长期生存的关键因素,现有技术可通过基因组、转录组测序解析耐药的分子特征,优势是能够高通量筛选潜在耐药相关分子,局限性是多数筛选得到的分子缺乏功能验证,且尚未形成可应用于临床的耐药预测标志物体系。在lncRNA研究领域,现有研究已证实lncRNA可通过表观遗传调控、转录后调控、作为miRNA海绵等多种方式参与肿瘤细胞的增殖、侵袭、耐药等过程,作为生物标志物具有组织特异性高、检测方便的优势,但多数lncRNA的功能具有组织和疾病亚型特异性,在他莫昔芬耐药乳腺癌中的作用尚未系统阐明。针对SOX2OT的现有研究显示,该lncRNA与SOX2基因位于同一基因组位点,在多种肿瘤中异常表达,且在乳腺癌中已被证实参与肿瘤干性调控,优势是已在多种肿瘤模型中得到验证,局限性是其在他莫昔芬耐药亚型中的表达变化和功能完全未知,且其与SOX2的调控关系在耐药背景下是否成立也尚未证实。本研究的创新价值在于首次采用两种不同构建方式的他莫昔芬耐药细胞系,系统验证SOX2OT的表达变化,同时结合临床组织样本和公共数据库数据,明确其作为预后和耐药预测标志物的潜力,且首次证实在耐药细胞中SOX2OT的功能不依赖于SOX2的表达调控,填补了领域内的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是明确lncRNA SOX2OT在他莫昔芬耐药乳腺癌中的生物学作用,核心科学问题包括SOX2OT是否参与他莫昔芬耐药的发生发展、其对耐药细胞恶性表型的调控机制、以及其与SOX2和肿瘤微环境的潜在关联,整体技术路线遵循“分子筛选→预后关联→功能验证→临床样本验证”的闭环逻辑,首先通过转录组筛选锁定差异表达分子,随后通过体外功能实验明确其生物学功能,最后结合临床样本验证研究结果的临床转化价值。
3.1 耐药细胞系构建与lncRNA差异表达筛选
该环节的核心实验目的是在他莫昔芬耐药乳腺癌细胞中筛选稳定差异表达的lncRNA,锁定后续研究的目标分子。实验采用两种独立构建的他莫昔芬耐药细胞系作为研究模型,其中TAMR-V细胞为长期暴露于他莫昔芬诱导构建的耐药株,TAMR-H细胞为商用的4-羟基他莫昔芬诱导耐药株,以luminal A型亲本MCF-7细胞为对照,首先通过下一代测序分析细胞系的分子特征,随后采用lncRNA qPCR芯片检测90种lncRNA的表达水平,筛选标准为表达变化倍数>2倍(上调)或<0.5倍(下调),后续采用实时荧光定量PCR(RT-qPCR)对候选分子的表达进行重复验证。实验结果显示,两种耐药细胞系中共有9种lncRNA呈现一致的表达变化,其中7SK、NTT、SOX2OT表达显著下调,其余6种lncRNA表达上调,结合已有文献报道的SOX2OT在乳腺癌中的潜在作用,最终锁定SOX2OT为研究对象,对应结果为图1的lncRNA表达谱。
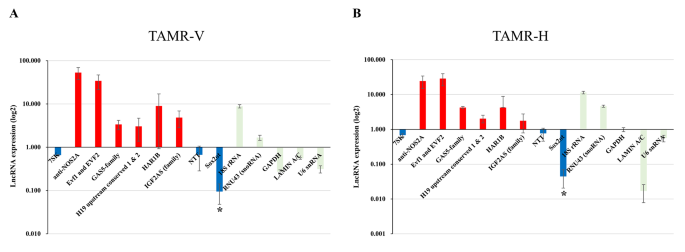
实验所用关键产品:System Biosciences的Human LncProfilers™ qPCR Array Kits、Takara的RNAiso Plus、Applied Biosystems的TaqMan Gene Expression Master Mix和Power SYBR Green PCR Master Mix。
3.2 SOX2OT表达与患者预后的关联分析
该环节的实验目的是分析SOX2OT及其关联分子SOX2的表达与HR阳性乳腺癌患者预后的相关性,为其作为预后标志物的潜力提供临床数据支持。实验采用Kaplan-Meier plotter公共数据库中的乳腺癌RNA测序数据集,分别纳入luminal A型和luminal B型乳腺癌患者的表达与生存数据,采用Log-rank检验分析表达水平与总生存期的关联。实验结果显示,在luminal A型乳腺癌患者中,SOX2OT高表达者的总生存期显著优于低表达者,风险比为0.30(P=0.0092,样本量文献未明确提供),luminal B型患者中同样呈现高表达预后更好的趋势,风险比为0.45(P=0.0020,样本量文献未明确提供);而SOX2的表达与两种亚型患者的总生存期均无显著统计学关联,对应结果为图2的Kaplan-Meier生存曲线。
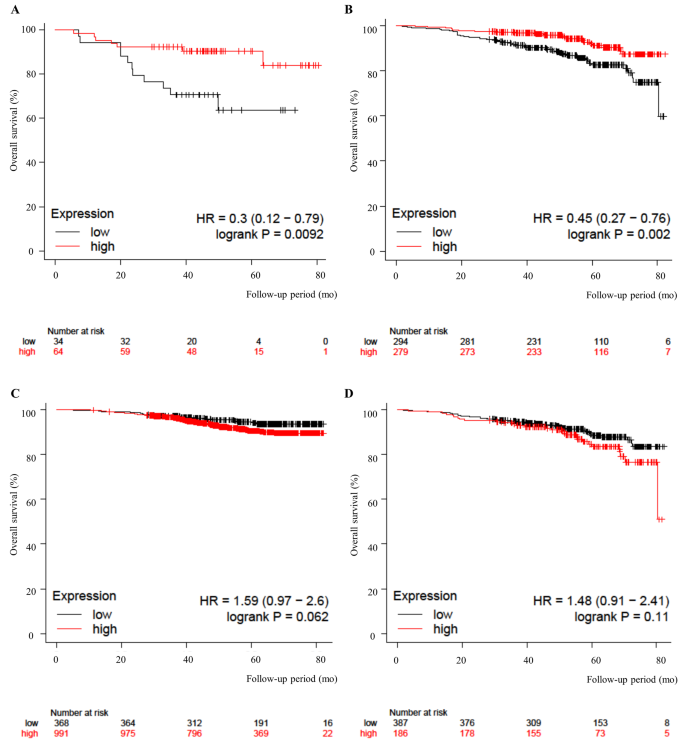
文献未提及该环节额外实验产品,领域常规使用生物信息学分析工具与公共数据库数据集。
3.3 SOX2OT过表达细胞模型构建与表达验证
该环节的实验目的是构建SOX2OT过表达的耐药细胞模型,验证过表达效率,并明确SOX2OT对SOX2表达的调控关系。实验通过分子克隆将SOX2OT的cDNA片段插入pcDNA3.1过表达载体,采用Lipofectamine™ RNAiMAX转染试剂将过表达载体或空白对照载体分别转入TAMR-V和TAMR-H细胞,转染48小时后提取细胞总RNA,采用RT-qPCR检测SOX2OT和SOX2的相对表达水平,以GAPDH和β-actin作为内参基因,采用2−ΔΔCT法计算相对表达量。实验结果显示,转染过表达载体后,两种耐药细胞中SOX2OT的表达水平较对照组显著升高,而SOX2的表达水平无明显变化,提示在他莫昔芬耐药细胞中SOX2OT不直接调控SOX2的转录表达,对应结果为图3的载体构建示意图、琼脂糖凝胶电泳验证图以及图4的基因表达定量结果。
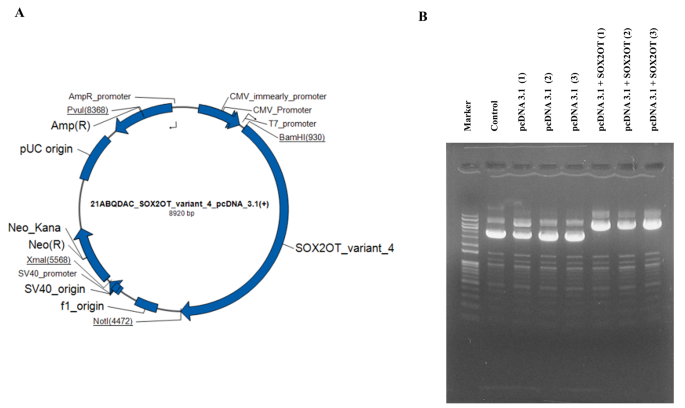
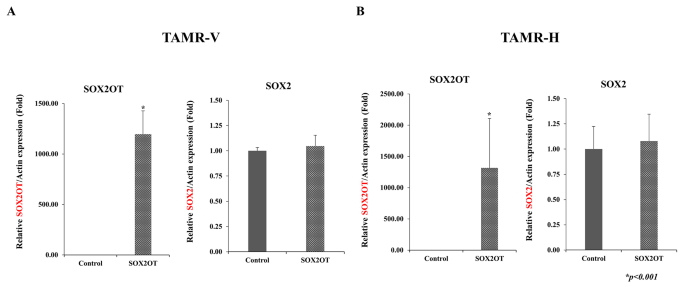
实验所用关键产品:Thermo Fisher Scientific的pcDNA3.1载体、Lipofectamine™ RNAiMAX转染试剂。
3.4 SOX2OT过表达对细胞增殖的影响检测
该环节的实验目的是明确SOX2OT过表达对他莫昔芬耐药细胞增殖能力和他莫昔芬敏感性的影响。实验将转染后的TAMR-V、TAMR-H细胞和亲本MCF-7细胞接种于96孔板,分别给予不同浓度的他莫昔芬或4-羟基他莫昔芬处理48小时,采用MTT法检测细胞活力,每组实验设置3个复孔,独立重复3次,采用Student’s t检验分析组间差异。实验结果显示,20μM他莫昔芬处理后,MCF-7细胞活力显著降低,而TAMR-V和TAMR-H细胞活力无明显下降,证实两种耐药细胞系的耐药特性稳定;SOX2OT过表达后,两种耐药细胞的活力均较对照组升高,其中TAMR-H细胞的升高具有统计学显著性(细胞活力升高幅度文献未明确提供,P<0.001,n=3),对应结果为图5的MTT检测结果。
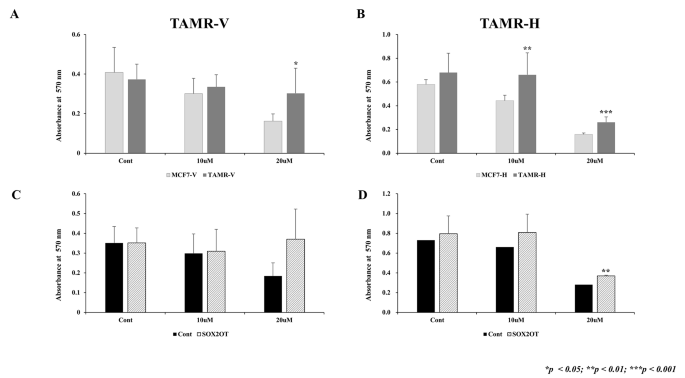
实验所用关键产品:Sigma-Aldrich的他莫昔芬、4-羟基他莫昔芬,Agilent Technologies的微孔板分光光度计。
3.5 SOX2OT过表达对细胞迁移和侵袭的影响检测
该环节的实验目的是探究SOX2OT过表达对他莫昔芬耐药细胞迁移和侵袭能力的调控作用。细胞迁移能力采用伤口愈合实验检测,转染后的细胞接种于6孔板,待细胞融合度达到90%以上时用无菌枪头划痕,分别在0、48、72小时拍摄划痕区域,采用ImageJ软件计算伤口愈合率;细胞侵袭能力采用Matrigel包被的Transwell小室实验检测,转染后的细胞用无血清培养基重悬后接种于上室,下室加入含10%胎牛血清的完全培养基作为趋化因子,培养48小时后固定、染色并计数穿过基质胶的细胞数量,每组实验独立重复3次。实验结果显示,Transwell侵袭实验中SOX2OT过表达组的TAMR-V和TAMR-H细胞侵袭数量较对照组有升高趋势,但未达到统计学显著性;伤口愈合实验显示,耐药细胞的基础迁移能力与MCF-7细胞无明显差异,SOX2OT过表达对细胞迁移能力无显著调控作用,对应结果为图6的侵袭和迁移实验结果。
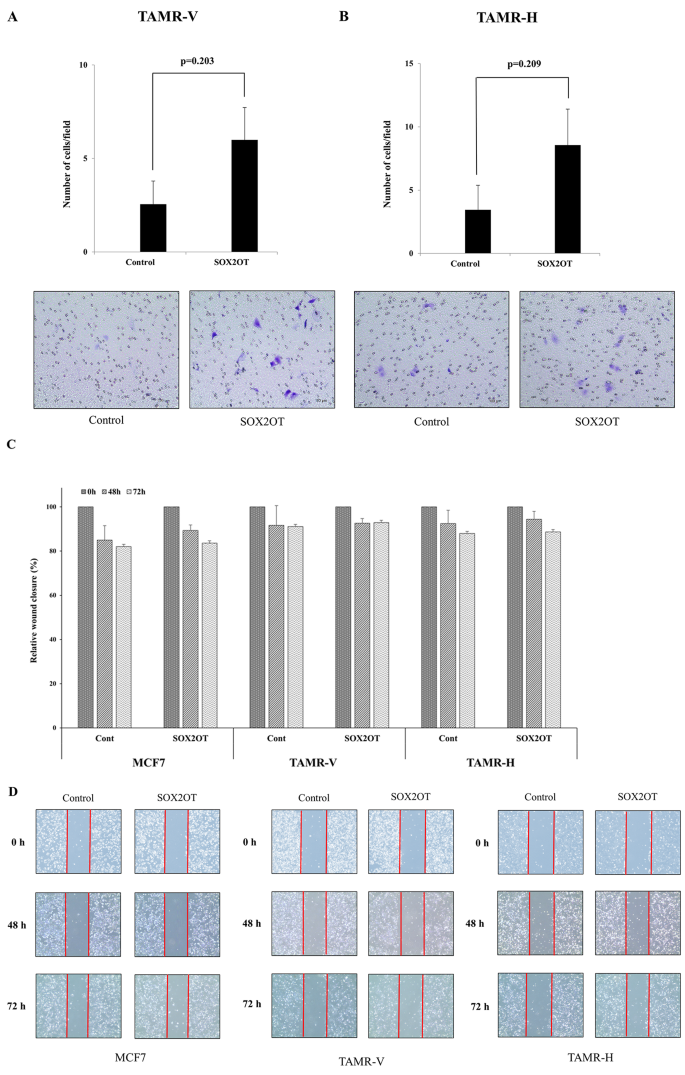
实验所用关键产品:Corning Inc.的Matrigel基质胶、Transwell小室,Olympus的显微镜成像系统。
3.6 不同乳腺癌亚型组织中SOX2OT的表达检测
该环节的实验目的是验证细胞系中观察到的SOX2OT表达下调在临床耐药组织中是否一致,提升研究结果的临床转化价值。实验收集不同分子亚型的乳腺癌临床组织样本,包括luminal A型、luminal B型、三阴性乳腺癌和他莫昔芬耐药乳腺癌组织,提取组织总RNA后采用RT-qPCR检测SOX2OT的相对表达水平。实验结果显示,SOX2OT在luminal B型乳腺癌组织中表达最高,在他莫昔芬耐药乳腺癌组织中表达显著下调,且表达水平低于三阴性乳腺癌组织,与细胞系中的表达变化趋势完全一致,对应结果为图7的组织表达定量结果。
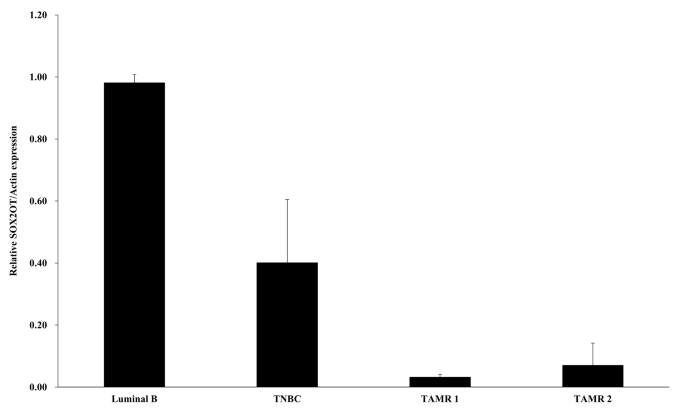
文献未提及该环节具体实验产品,领域常规使用组织RNA提取试剂、RT-qPCR相关试剂。
4. Biomarker 研究及发现成果
本研究涉及的生物标志物(Biomarker)为长链非编码RNA SOX2OT,属于非编码RNA类生物标志物,其筛选验证遵循“细胞系转录组筛选→公共数据库预后关联→临床组织样本验证→体外功能验证”的完整逻辑链条,明确了其在他莫昔芬耐药乳腺癌中的表达特征和临床价值。
SOX2OT的检测样本涵盖体外培养的乳腺癌细胞系和临床乳腺癌组织两类,细胞系样本包括亲本MCF-7细胞、两种他莫昔芬耐药细胞,临床样本包括不同分子亚型的乳腺癌组织和他莫昔芬耐药组织,验证方法为RT-qPCR定量检测表达水平。预后分析数据显示,在luminal A型乳腺癌中,SOX2OT高表达患者的死亡风险较低表达患者降低70%(风险比HR=0.30,P=0.0092,95%置信区间文献未明确提供);在luminal B型乳腺癌中,SOX2OT高表达患者的死亡风险降低55%(HR=0.45,P=0.0020,95%置信区间文献未明确提供)。在他莫昔芬耐药细胞系中,SOX2OT的表达水平较亲本MCF-7细胞降低超过50%(表达变化<0.5倍,P<0.05,n=3),在耐药临床组织中同样呈现显著下调的特征。
核心成果方面,SOX2OT可作为HR阳性乳腺癌患者的预后标志物,高表达提示更好的总生存期;同时其在他莫昔芬耐药细胞和组织中的特异性下调,使其具备作为他莫昔芬耐药预测标志物的潜力。本研究的创新性在于首次证实SOX2OT在他莫昔芬耐药乳腺癌中的表达下调,且其对耐药细胞增殖、侵袭的调控作用不依赖于SOX2的表达调控,打破了既往研究中SOX2OT与SOX2共调控的固有认知,为内分泌耐药的分子机制解析提供了新的方向。统计学结果显示,SOX2OT与luminal A型患者预后的关联P=0.0092,与luminal B型患者预后的关联P=0.0020,过表达后TAMR-H细胞增殖升高的统计学差异P<0.001,细胞侵袭实验的结果未达到统计学显著性。推测:SOX2OT对耐药细胞恶性表型的调控可能需要依赖肿瘤微环境中的其他因子共同作用,后续可通过共培养模型或动物实验进一步验证其在体内的功能和调控机制。