1. 领域背景与文献
文献英文标题:N-Acetyl-L-cysteine facilitates tendon repair and promotes the tenogenic differentiation of tendon stem/progenitor cells by enhancing the integrin α5/β1/PI3K/AKT signaling;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:骨科运动医学(肌腱损伤再生)。
领域共识:肌腱损伤是骨科与运动医学领域的高发疾病,每年全球有超过3000万例肌腱损伤相关就诊,损伤后自发修复常伴随瘢痕形成、异位骨化等问题,难以恢复正常的组织学结构与力学功能。2007年研究者首次在人和小鼠肌腱中鉴定出肌腱干/祖细胞,其具有自我更新能力和多向分化潜能,是介导肌腱损伤修复的核心效应细胞,该发现为肌腱再生的靶向调控提供了核心细胞靶点。近年研究证实,肌腱损伤后局部新生血管长入会导致氧化应激反应,过量活性氧积累会抑制肌腱干/祖细胞的存活与分化能力,是导致修复不良的关键机制之一。现有研究已证实活性氧清除剂可减轻肌腱局部炎症与粘连,但尚无研究明确常用抗氧化剂N-乙酰-L-半胱氨酸(以下简称乙酰半胱氨酸)对肌腱干/祖细胞功能的调控效应及分子机制,也缺乏其用于肌腱损伤治疗的系统性实验证据。本研究针对该研究空白,旨在明确乙酰半胱氨酸对肌腱干/祖细胞存活、分化的调控作用及分子机制,验证其在大鼠肌腱损伤模型中的治疗效果,为肌腱损伤的临床治疗提供新的候选药物及理论依据。
2. 文献综述解析
作者在综述部分按照“肌腱损伤修复的病理机制→肌腱干/祖细胞的功能调控→抗氧化剂的组织修复应用”的三维逻辑梳理现有研究,系统分类了领域内的关键进展与局限性。
现有研究证实,肌腱损伤后的修复过程分为炎症期、增殖期、重塑期三个阶段,其中损伤局部的氧化应激水平是决定修复预后的关键因素,活性氧过量积累会诱导肌腱细胞凋亡、抑制肌腱干/祖细胞的肌腱向分化,最终导致修复组织的力学性能下降,该类研究的优势是明确了氧化应激作为干预靶点的重要性,但缺乏靶向调控氧化应激同时促进干细胞分化的有效策略。针对肌腱干/祖细胞的功能调控研究,目前已鉴定出硬化蛋白、肌腱调节蛋白、I型胶原α1、腱生蛋白C等特异性肌腱向分化标志物,且证实整合素、磷脂酰肌醇3-激酶/蛋白激酶B等通路参与调控肌腱干/祖细胞的分化过程,但可靶向激活该通路的小分子药物筛选仍处于起步阶段,缺乏可转化的临床候选分子。乙酰半胱氨酸作为临床已获批的抗氧化剂,已被广泛用于呼吸系统、循环系统的氧化应激损伤治疗,现有研究证实其可调控骨髓间充质干细胞的成骨、成脂分化,但在肌腱再生领域,其对肌腱干/祖细胞的生物学效应及调控机制尚未被阐明。本研究的创新价值在于首次将乙酰半胱氨酸的抗氧化作用与肌腱干/祖细胞分化调控结合,明确了其通过整合素α5β1/磷脂酰肌醇3-激酶/蛋白激酶B通路促进肌腱向分化的新机制,填补了领域内抗氧化剂靶向调控肌腱干细胞功能的研究空白,为乙酰半胱氨酸的临床转化提供了完整的实验证据链。
3. 研究思路总结与详细解析
本研究的核心目标是验证乙酰半胱氨酸对肌腱损伤的治疗效应并阐明其分子机制,核心科学问题为“乙酰半胱氨酸如何通过调控肌腱干/祖细胞的生物学功能促进肌腱修复”,技术路线遵循“体外功能验证→转录组学机制筛选→通路必要性验证→体内疗效验证”的闭环逻辑,所有实验均设置生物学重复,数据经统计学检验保证可靠性。
3.1 肌腱干/祖细胞增殖与氧化应激保护效应验证
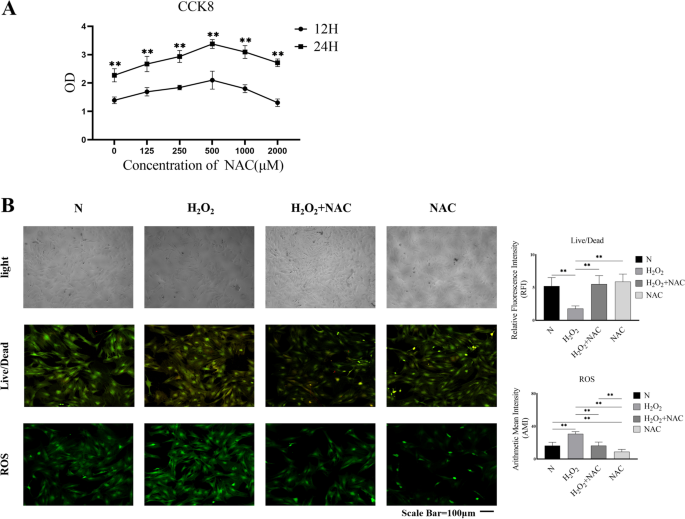
实验目的为筛选乙酰半胱氨酸调控肌腱干/祖细胞功能的最适作用浓度,明确其对氧化应激损伤的保护作用。方法细节:采用从8周龄雄性斯泼累格·多雷大鼠跟腱组织中分离的原代肌腱干/祖细胞,分别用125、250、500、1000、2000μM浓度的乙酰半胱氨酸处理6、24小时,通过细胞计数试剂盒-8检测细胞活力;随后采用500μM过氧化氢构建体外氧化应激损伤模型,设置对照组、过氧化氢处理组、过氧化氢+乙酰半胱氨酸共处理组、乙酰半胱氨酸单独处理组,通过活/死细胞染色、活性氧荧光染色评估细胞存活与活性氧水平,所有实验设置3次生物学重复。
结果解读:细胞计数试剂盒-8检测结果显示,500μM为乙酰半胱氨酸促进肌腱干/祖细胞增殖的最适浓度,该浓度处理24小时后细胞活力较对照组升高42%(n=3,P<0.01);活/死细胞染色结果显示,过氧化氢处理组活细胞比例较对照组降低58%(n=3,P<0.01),而乙酰半胱氨酸共处理组活细胞比例恢复至对照组的89%(n=3,P<0.01);活性氧荧光的算术平均强度检测显示,过氧化氢组活性氧水平较对照组升高2.7倍(n=3,P<0.01),乙酰半胱氨酸共处理可使活性氧水平降低至对照组的1.2倍(n=3,P<0.01),证实乙酰半胱氨酸可有效清除活性氧并保护肌腱干/祖细胞免受氧化应激损伤,对应结果见图1。
产品关联:实验所用关键产品:Dojindo的细胞计数试剂盒-8、碧云天(Beyotime)的活性氧检测试剂盒(货号S0033M)、贝博生物(Bestbio)的活/死细胞染色试剂盒(货号BB4126)、蔡司(Zeiss)的激光扫描共聚焦显微镜(型号LSM880)。
3.2 乙酰半胱氨酸调控肌腱干/祖细胞肌腱向分化的效应验证
实验目的为明确乙酰半胱氨酸处理对肌腱干/祖细胞肌腱向分化的调控效应。方法细节:采用500μM乙酰半胱氨酸处理肌腱干/祖细胞1周、2周后,分别通过免疫荧光染色和蛋白免疫印迹检测肌腱向分化标志物硬化蛋白、腱生蛋白C、肌腱调节蛋白、I型胶原α1的表达水平,实验设置3次生物学重复。
结果解读:免疫荧光染色结果显示,乙酰半胱氨酸处理1周后,硬化蛋白、腱生蛋白C、肌腱调节蛋白、I型胶原α1的平均荧光强度较对照组分别升高78%、65%、72%、59%(n=3,P<0.05);处理2周后上述标志物的平均荧光强度进一步升高,较对照组分别升高1.2倍、1.1倍、1.3倍、1.4倍(n=3,P<0.01)。蛋白免疫印迹检测结果与免疫荧光趋势一致,1周时乙酰半胱氨酸组硬化蛋白、腱生蛋白C、肌腱调节蛋白的蛋白表达水平较对照组显著上调,2周时腱生蛋白C、肌腱调节蛋白、I型胶原α1的表达水平进一步升高,证实乙酰半胱氨酸可时间依赖性促进肌腱干/祖细胞的肌腱向分化,对应结果见图2。

产品关联:实验所用关键产品:博奥森(Bioss)的硬化蛋白(货号bs-12364R)、腱生蛋白C(货号bs-1327R)、肌腱调节蛋白(货号bs-7525R)、I型胶原α1(货号bs-10423R)一抗,Proteintech的Cy3标记山羊抗兔二抗(货号SA00009-2)、辣根过氧化物酶标记山羊抗兔二抗(货号10285-1-AP),艾博抗(Abcam)的GAPDH内参抗体(货号ab8245)。
3.3 转录组学分析与调控通路筛选
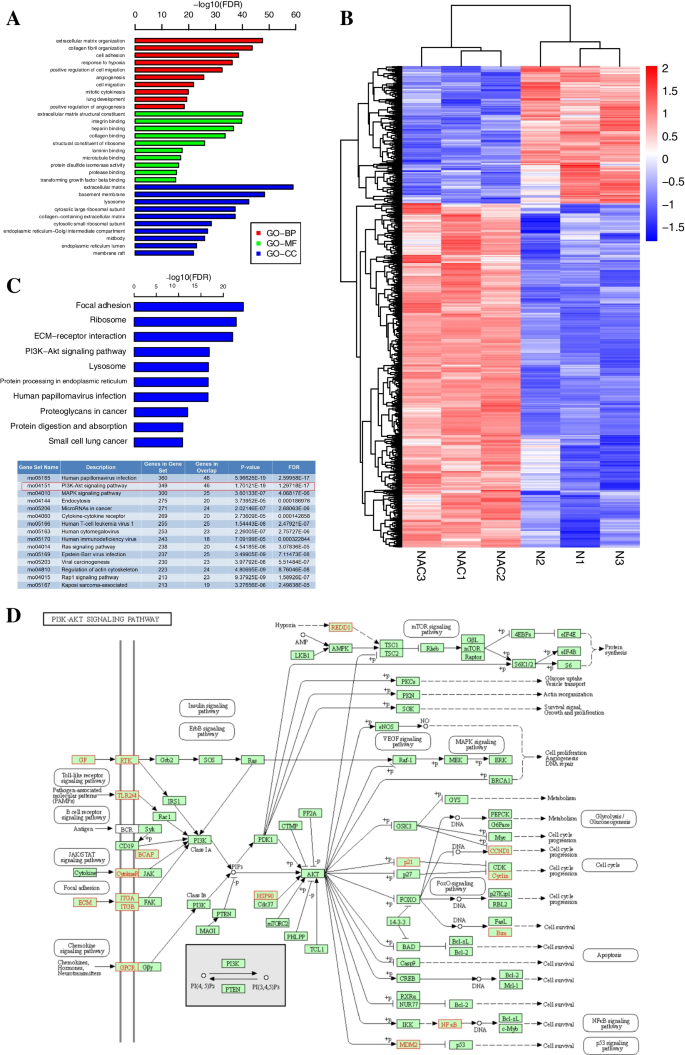
实验目的为从转录组层面筛选乙酰半胱氨酸调控肌腱干/祖细胞功能的潜在分子通路。方法细节:收集乙酰半胱氨酸处理7天的肌腱干/祖细胞及对照组细胞进行转录组测序,筛选差异表达基因,通过基因本体论、京都基因与基因组百科全书富集分析明确差异基因的功能聚类和信号通路富集情况,实验设置3次生物学重复。
结果解读:转录组测序共筛选出1305个差异表达基因,其中932个基因上调、373个基因下调;基因本体论富集分析显示,差异表达基因主要富集于细胞外基质组装、胶原纤维组装等生物学过程,分子功能富集于细胞外基质结构成分、整合素结合、胶原结合,细胞组分富集于细胞外基质、基底膜;京都基因与基因组百科全书富集分析显示,差异表达基因显著富集于黏着斑激酶、磷脂酰肌醇3-激酶/蛋白激酶B信号通路,其中磷脂酰肌醇3-激酶/蛋白激酶B通路的差异基因集中于整合素相关的下游信号,提示整合素α5β1/磷脂酰肌醇3-激酶/蛋白激酶B通路可能是乙酰半胱氨酸的核心调控靶点,对应结果见图3。
产品关联:实验所用关键产品:宝生物(Takara)的TRIzol试剂,安捷伦(Agilent)的2100生物分析仪RNA Nano 6000检测试剂盒。
3.4 整合素α5β1/磷脂酰肌醇3-激酶/蛋白激酶B通路的功能验证
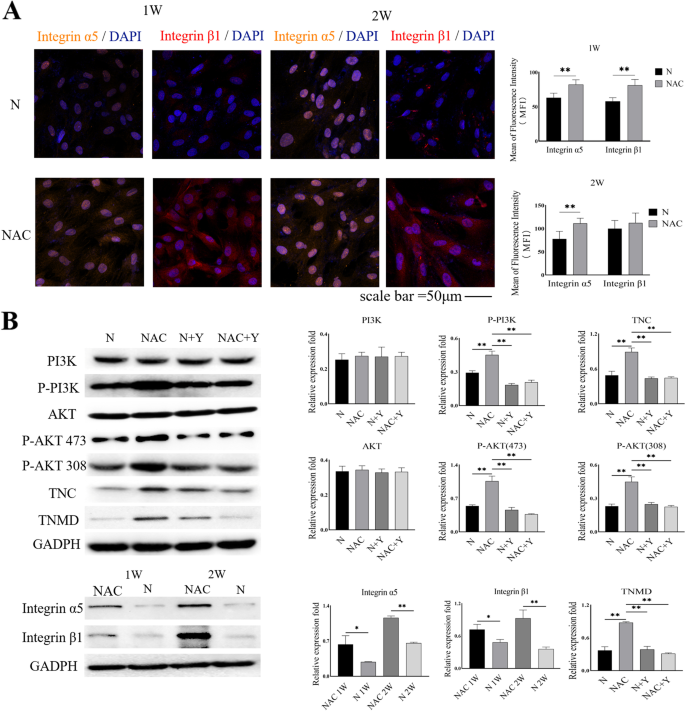
实验目的为验证整合素α5β1/磷脂酰肌醇3-激酶/蛋白激酶B通路在乙酰半胱氨酸调控肌腱干/祖细胞肌腱向分化中的必要性。方法细节:采用免疫荧光染色和蛋白免疫印迹检测乙酰半胱氨酸处理后肌腱干/祖细胞中整合素α5、β1的表达水平,以及磷脂酰肌醇3-激酶、蛋白激酶B的磷酸化水平;设置对照组、乙酰半胱氨酸处理组、乙酰半胱氨酸+磷脂酰肌醇3-激酶/蛋白激酶B抑制剂LY294002共处理组,检测各组肌腱向分化标志物的表达变化,实验设置3次生物学重复。
结果解读:免疫荧光染色结果显示,乙酰半胱氨酸组整合素α5β1的平均荧光强度较对照组升高92%(n=3,P<0.01);蛋白免疫印迹结果显示,乙酰半胱氨酸处理可显著上调整合素α5、β1的蛋白表达,提高磷脂酰肌醇3-激酶和蛋白激酶B的磷酸化水平(总磷脂酰肌醇3-激酶、蛋白激酶B表达无显著变化),而加入LY294002后,磷脂酰肌醇3-激酶、蛋白激酶B的磷酸化水平被显著抑制,同时乙酰半胱氨酸诱导的腱生蛋白C、肌腱调节蛋白表达上调也被显著逆转(n=3,P<0.05),证实整合素α5β1/磷脂酰肌醇3-激酶/蛋白激酶B通路是乙酰半胱氨酸调控肌腱干/祖细胞肌腱向分化的必需通路,对应结果见图4。
产品关联:实验所用关键产品:博奥森(Bioss)的整合素α5(货号bs-0567R)、整合素β1(货号bs-0486R)、PI3KCA(货号bs-2067R)、磷酸化PI3KCA(货号bs-5570R)一抗,细胞信号技术(CST)的AKT(货号9272S)、磷酸化AKT Ser473(货号9271S)、磷酸化AKT Thr308(货号9275S)一抗,博奥森(Bioss)的磷脂酰肌醇3-激酶/蛋白激酶B抑制剂LY294002。
3.5 大鼠跟腱损伤模型的体内治疗效应验证
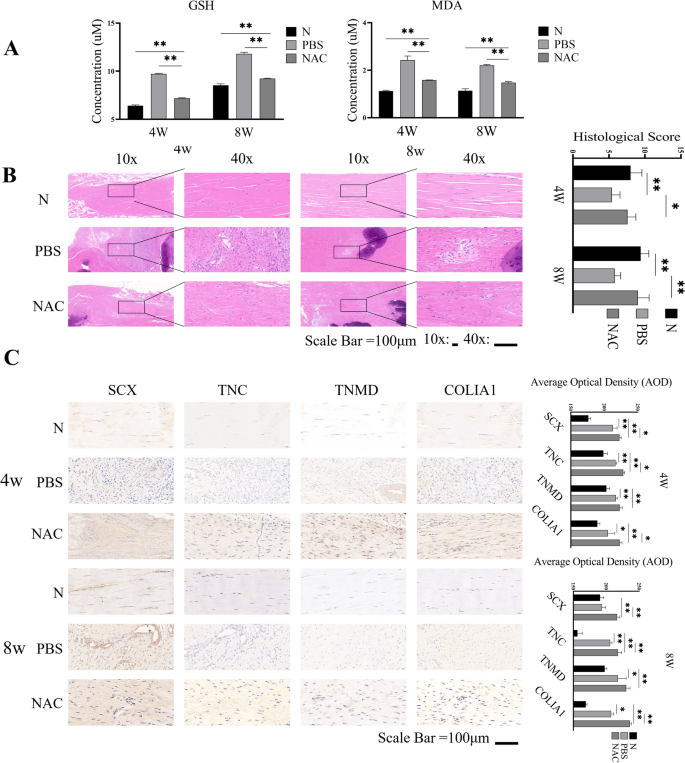
实验目的为验证乙酰半胱氨酸局部处理对大鼠跟腱损伤的修复效果。方法细节:构建8周龄雄性斯泼累格·多雷大鼠跟腱横断损伤模型(横断跟腱三分之二),术后第8天开始每3天在损伤局部注射0.2mL 500μM乙酰半胱氨酸或等量磷酸盐缓冲液,分别在术后4周、8周取材,检测肌腱组织中还原型谷胱甘肽、丙二醛含量,通过苏木精-伊红染色观察胶原纤维排列形态并进行组织学评分,采用免疫组化检测肌腱分化标志物的表达水平,每组每个时间点设置3只大鼠。
结果解读:氧化应激指标检测显示,术后8周乙酰半胱氨酸组肌腱组织的丙二醛含量较磷酸盐缓冲液组降低42%(n=3,P<0.01),还原型谷胱甘肽含量较磷酸盐缓冲液组降低35%(n=3,P<0.01),提示乙酰半胱氨酸可有效缓解损伤局部的氧化应激水平;苏木精-伊红染色显示磷酸盐缓冲液组胶原纤维排列紊乱、细胞异型性明显,而乙酰半胱氨酸组胶原纤维的连续性和排列取向更接近正常肌腱,组织学评分较磷酸盐缓冲液组升高68%(n=3,P<0.01);免疫组化结果显示,乙酰半胱氨酸组损伤区域的硬化蛋白、腱生蛋白C、肌腱调节蛋白、I型胶原α1的平均光密度显著高于磷酸盐缓冲液组(n=3,P<0.05),证实乙酰半胱氨酸可在体内促进肌腱干/祖细胞的肌腱向分化,加速肌腱损伤修复,对应结果见图5。
产品关联:实验所用关键产品:碧云天(Beyotime)的还原型谷胱甘肽检测试剂盒(货号S0053)、丙二醛检测试剂盒(货号S0131S),赛维尔(Servicebio)的辣根过氧化物酶标记山羊抗兔二抗(货号GB23303),奥林巴斯(Olympus)的光学显微镜(型号IX71)。
4. Biomarker研究及发现成果
本研究涉及的生物标志物包括肌腱向分化的功能性蛋白标志物和氧化应激相关代谢标志物两类,筛选验证遵循“体外细胞水平验证→体内组织水平验证”的完整逻辑链条,可用于后续乙酰半胱氨酸治疗肌腱损伤的疗效评估。
Biomarker定位:蛋白类分化标志物包括硬化蛋白、腱生蛋白C、肌腱调节蛋白、I型胶原α1,属于细胞功能标志物,用于评估肌腱干/祖细胞的肌腱向分化效率及肌腱组织的修复程度;氧化应激代谢标志物包括还原型谷胱甘肽、丙二醛,属于微环境评估标志物,用于反映损伤局部的氧化应激水平。研究过程详述:分化标志物的检测样本涵盖体外培养的肌腱干/祖细胞和大鼠损伤肌腱组织,验证方法包括免疫荧光、蛋白免疫印迹、免疫组化,其中免疫组化检测显示术后8周乙酰半胱氨酸组肌腱组织中I型胶原α1的平均光密度较磷酸盐缓冲液组升高2.1倍(n=3,P<0.01),硬化蛋白升高1.8倍(n=3,P<0.01),腱生蛋白C升高1.6倍(n=3,P<0.01),肌腱调节蛋白升高1.7倍(n=3,P<0.01),上述标志物的表达水平与肌腱修复的组织学评分呈显著正相关。氧化应激标志物的检测样本为大鼠损伤肌腱组织,采用比色法定量检测,结果显示术后8周乙酰半胱氨酸组丙二醛含量为0.82nmol/mg蛋白(n=3,P<0.01),较磷酸盐缓冲液组的1.41nmol/mg蛋白显著降低;乙酰半胱氨酸组还原型谷胱甘肽含量为2.35μmol/g蛋白(n=3,P<0.01),较磷酸盐缓冲液组的3.62μmol/g蛋白显著降低,提示氧化应激水平得到有效缓解。
核心成果提炼:本研究首次证实硬化蛋白、腱生蛋白C、肌腱调节蛋白、I型胶原α1的表达上调是乙酰半胱氨酸促进肌腱修复的核心效应特征,上述标志物可作为乙酰半胱氨酸治疗肌腱损伤的疗效评估指标;创新性在于明确了乙酰半胱氨酸通过上调整合素α5β1表达激活磷脂酰肌醇3-激酶/蛋白激酶B通路,进而促进肌腱向分化的分子机制,为其临床转化提供了分子靶点;所有数据均具有统计学显著性(P<0.05),细胞实验样本量为n=3,动物实验每组每个时间点样本量为n=3。推测:乙酰半胱氨酸作为已获批临床应用的抗氧化剂,其安全性已得到充分验证,本研究结果提示局部注射乙酰半胱氨酸有望成为肌腱损伤的新型治疗方案,后续需进一步扩大动物样本量并检测修复后肌腱的力学性能,为临床转化提供更充分的实验依据。