1. 领域背景与文献
文献英文标题:MicroRNA-338-3p alleviates lipopolysaccharide-induced inflammatory damage in HK-2 cells;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:炎症性肾损伤分子机制研究。
领域共识:脓毒症是宿主对感染应答失调导致的全身炎症反应综合征,急性肾损伤是脓毒症住院患者的常见并发症,与患者死亡率升高直接相关。目前研究已证实,肾近端小管上皮细胞分泌的IL-1β、IL-6、IL-8、TNF-α等炎症因子渗透至肾间质后会进一步加重肾功能损伤,NF-κB、p38 MAPK通路是调控炎症因子生成的核心通路,氧化应激与炎症的协同作用会加速肾功能衰退。microRNA作为长度为20~24个核苷酸的非编码RNA,可通过靶向结合mRNA的3"非翻译区调控其降解或翻译,是近年炎症疾病调控机制的研究热点,目前已有miR-103、miR-30b等多个microRNA被证实参与调控肾小管上皮细胞炎症损伤,但miR-338-3p在肾损伤中的功能与调控机制此前尚未被阐明。
本研究针对该研究空白,以脂多糖(LPS)诱导的人近端肾小管上皮HK-2细胞为炎症损伤模型,探究miR-338-3p对肾小管上皮细胞炎症损伤的调控作用,为脓毒症诱导急性肾损伤的诊断标志物筛选与治疗靶点开发提供新的研究方向。
2. 文献综述解析
作者的文献综述核心评述逻辑按“疾病机制→调控分子→目标分子功能”三层维度展开,首先梳理脓毒症急性肾损伤的病理生理机制,其次总结microRNA在炎症性疾病中的调控作用,最后聚焦miR-338-3p的已报道功能范围,定位研究空白。
现有研究的关键支持结论包括:miR-221、miR-222可抑制慢性炎症中的内皮细胞增殖与血管生成,miR-103可通过靶向C-Myc加重LPS诱导的HK-2细胞炎症损伤,miR-30b可促进LPS诱导的HK-2细胞炎症因子生成,miR-500A-3p具有抗炎特性可减轻肾损伤,miR-338-3p在对乙酰氨基酚诱导的急性肝损伤、LPS诱导的支气管上皮细胞炎症中均发挥抗炎作用。现有研究的局限性在于,已有的miR-338-3p功能研究仅覆盖神经退行性疾病、肝损伤、呼吸系统炎症等领域,完全未涉及肾损伤相关的功能与机制探索,且缺乏临床样本层面的表达验证数据。
本研究的创新价值在于首次明确了miR-338-3p在肾小管上皮细胞炎症损伤中的保护作用,首次在脓毒症肾损伤患者血清中验证了miR-338-3p的表达下调特征,填补了该分子在肾损伤领域的研究空白,为脓毒症急性肾损伤的机制研究提供了新的调控靶点。
3. 研究思路总结与详细解析
本研究的核心研究目标为明确miR-338-3p对LPS诱导的HK-2细胞炎症损伤的调控作用及下游分子机制,核心科学问题为miR-338-3p是否可通过调控炎症通路与凋亡通路缓解肾小管上皮细胞炎症损伤,技术路线遵循“临床样本验证→细胞模型表达分析→功能获得验证→机制探索”的逻辑闭环。
3.1 miR-338-3p表达特征验证
实验目的为明确脓毒症肾损伤状态及LPS处理下miR-338-3p的表达变化规律。方法细节:纳入脓毒症诱导急性肾损伤患者与健康志愿者,收集空腹外周静脉血分离血清,采用5μg/mL LPS处理HK-2细胞,分别设置不同LPS处理浓度梯度(0~10μg/mL)与不同处理时间梯度(12~48h),通过实时荧光定量聚合酶链反应(qRT-PCR)检测血清及细胞中miR-338-3p的表达水平。结果解读:对应图1的qRT-PCR检测结果,脓毒症肾损伤患者血清中miR-338-3p水平较健康志愿者显著降低(P<0.05),HK-2细胞中miR-338-3p水平随LPS处理浓度升高、处理时间延长呈梯度下调(P<0.05),证实LPS可负调控miR-338-3p的表达。
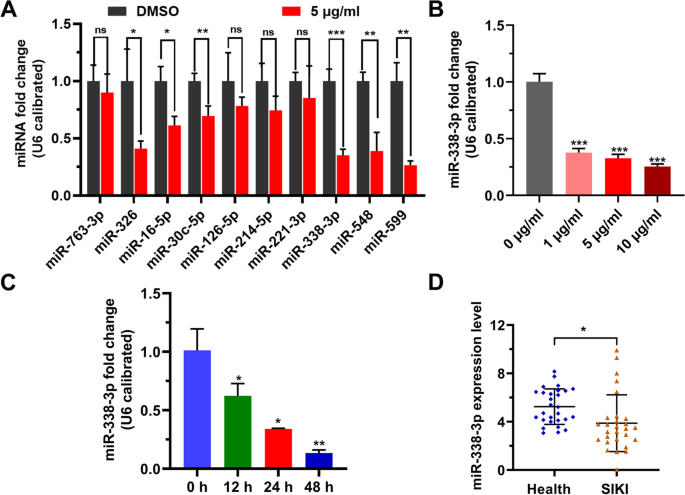
产品关联:实验所用关键产品:TIANGEN的血清miRNA提取试剂盒(货号DP503)、Takara的PrimeScript逆转录试剂盒(货号RR047A)、诺唯赞的SYBR Green qPCR Mix(货号Q111-02)。
3.2 miR-338-3p对细胞活力的调控作用验证
实验目的为明确上调miR-338-3p水平是否可缓解LPS诱导的HK-2细胞活力下降。方法细节:将HK-2细胞分为对照组、LPS处理组、LPS+模拟物阴性对照组、LPS+miR-338-3p模拟物组,转染200pmol miR-338-3p模拟物上调细胞内miR-338-3p水平,LPS处理24h后采用MTT法检测细胞活力。结果解读:对应图2的MTT检测结果,LPS处理可使HK-2细胞活力较对照组显著降低(P<0.0001),过表达miR-338-3p可使细胞活力较LPS组显著回升(P<0.05),证实miR-338-3p可缓解LPS诱导的细胞增殖抑制。

产品关联:文献未提及MTT试剂具体品牌,领域常规使用噻唑蓝类细胞活力检测试剂。
3.3 miR-338-3p抗炎功能验证
实验目的为明确miR-338-3p对LPS诱导的炎症因子表达的调控作用。方法细节:各组细胞处理24h后,分别收集细胞沉淀与细胞上清,采用qRT-PCR检测IL-1β、IL-6、IL-8、TNF-α的mRNA水平,采用酶联免疫吸附实验(ELISA)检测上清中上述炎症因子的蛋白水平。结果解读:对应图3的检测结果,LPS处理可使IL-1β、IL-6、IL-8、TNF-α的mRNA和蛋白水平较对照组显著升高(P<0.001),过表达miR-338-3p可使上述炎症因子水平较LPS组显著降低(P<0.01),证实miR-338-3p在HK-2细胞中发挥抗炎作用。
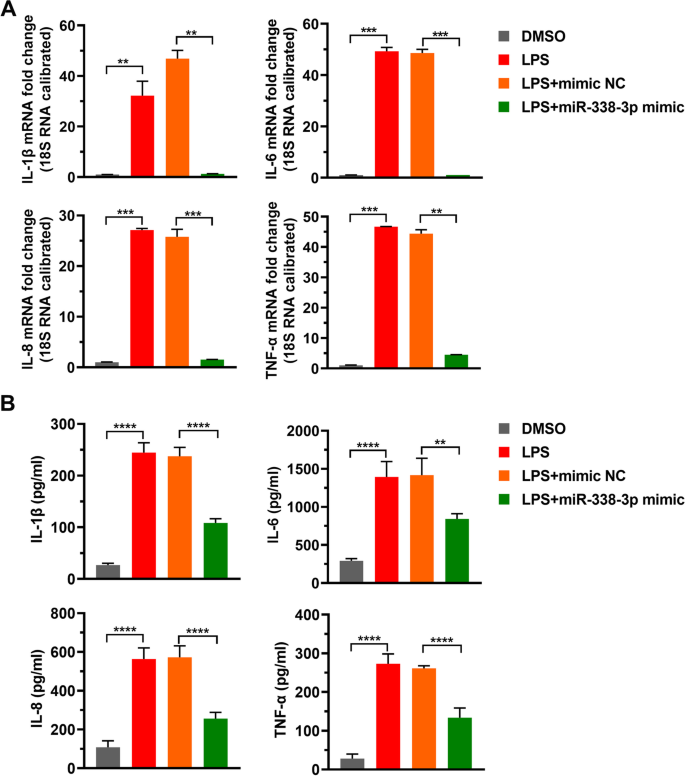
产品关联:实验所用关键产品:R&D Systems的IL-1β ELISA试剂盒(货号DY201-05)、IL-6 ELISA试剂盒(货号D6050)、IL-8 ELISA试剂盒(货号D8000C)、TNF-α ELISA试剂盒(货号DTA00D)。
3.4 miR-338-3p调控机制验证
实验目的为明确miR-338-3p缓解LPS诱导损伤的下游分子机制。方法细节:各组细胞处理24h后,采用JC-1染色结合流式细胞术检测线粒体膜电位,采用 Annexin V-FITC/PI双染结合流式细胞术检测细胞凋亡率,采用蛋白免疫印迹(Western Blot,WB)检测p38、p65、磷酸化p38、磷酸化p65、Bcl-2、Bax、cleaved caspase-3、cleaved caspase-9的蛋白水平,采用qRT-PCR检测Bcl-2、Bax的mRNA水平。结果解读:对应图4、图5的检测结果,LPS处理可使线粒体膜电位显著降低、细胞凋亡率显著升高(P<0.001),p38、p65磷酸化水平升高,抗凋亡蛋白Bcl-2的mRNA和蛋白水平降低、促凋亡蛋白Bax的mRNA和蛋白水平、cleaved caspase-3、cleaved caspase-9的蛋白水平升高;过表达miR-338-3p可逆转上述所有变化(P<0.05),证实miR-338-3p通过抑制p38 MAPK/NF-κB通路激活、抑制线粒体凋亡通路发挥细胞保护作用。
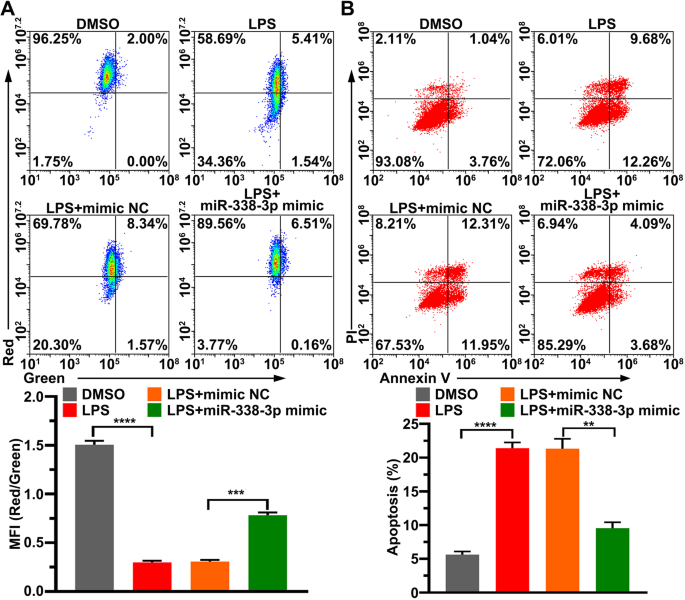
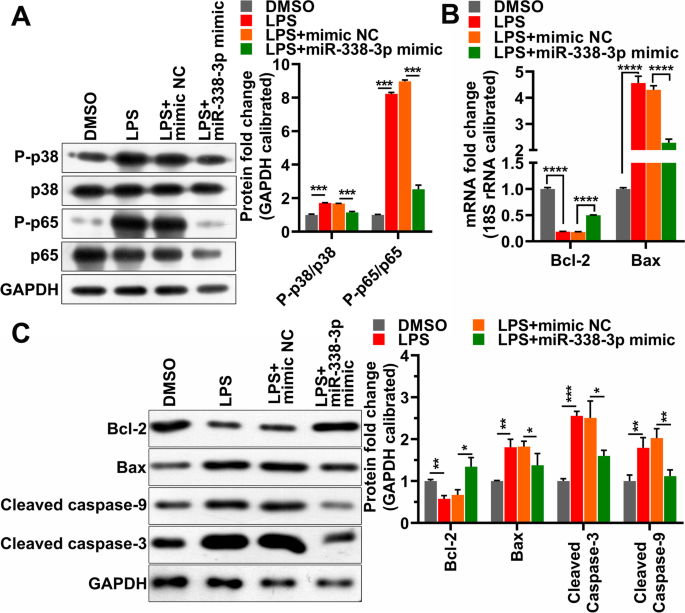
产品关联:实验所用关键产品:碧云天的JC-1染色试剂盒(货号C2006)、诺唯赞的凋亡检测试剂盒(货号A211-01)、Proteintech的Bcl-2抗体(货号12789-1-AP)、Bax抗体(货号50599-2-Ig)、Abcam的cleaved caspase-3抗体(货号ab32042)、cleaved caspase-9抗体(货号ab2324)。
4. Biomarker研究及发现成果
本研究涉及的Biomarker为循环miR-338-3p,筛选验证逻辑为:首先在LPS处理的HK-2细胞中筛选差异表达的microRNA,锁定miR-338-3p为候选分子,随后在脓毒症肾损伤患者血清样本中验证其表达变化,最后在细胞层面验证其功能与调控机制,逻辑链条完整。
该Biomarker的来源为脓毒症肾损伤患者外周血清、LPS处理的HK-2细胞,验证方法为qRT-PCR,检测结果显示脓毒症肾损伤患者血清miR-338-3p水平较健康对照显著降低(P<0.05),细胞水平验证LPS可浓度依赖性、时间依赖性降低HK-2细胞中miR-338-3p的表达,目前暂未开展诊断效能相关的ROC曲线分析,敏感性与特异性数据尚未明确。
核心成果方面,miR-338-3p可作为脓毒症诱导急性肾损伤的潜在诊断Biomarker,同时可作为抗炎治疗的潜在靶点,其功能为抑制p38 MAPK/NF-κB通路激活,减少炎症因子分泌,同时通过调控Bcl-2/Bax表达、抑制caspase家族剪切,减少线粒体途径的细胞凋亡,最终缓解肾小管上皮细胞炎症损伤。本研究首次发现miR-338-3p在肾损伤中的保护作用,创新性明确了其抗炎、抗凋亡的双重调控功能,为后续脓毒症急性肾损伤的诊断与治疗研究提供了新的靶点方向。推测:miR-338-3p在体内脓毒症肾损伤动物模型中也可能发挥保护作用,需后续动物实验进一步验证,其直接调控的下游靶基因也有待进一步探索。