1. 领域背景与文献
文献英文标题:Physical and functional interaction between the dyslexia candidate genes DYX1C1 and DCDC2;发表期刊:BMC Molecular and Cell Biology;影响因子:未公开;研究领域:神经发育遗传学、纤毛生物学。
发育性阅读障碍是最常见的神经发育类学习障碍,其遗传特性已被广泛证实,目前已鉴定出多个阅读障碍易感基因,其中诵读困难易感基因1(DYX1C1)与双皮质素结构域包含蛋白2(DCDC2)是重复验证次数最多的两个候选基因。领域共识:二者均被证实参与神经元迁移、纤毛生长与功能调控,属于细胞骨架互作蛋白,同时被归类为纤毛病相关基因,纤毛功能异常与精神分裂症、自闭症等多种神经精神疾病的发生密切相关。当前该领域尚未解决的核心问题为DYX1C1与DCDC2的具体分子功能未完全阐明,二者是否存在遗传及蛋白水平的相互作用、是否通过共同通路调控神经发育及纤毛功能的机制尚不清晰。本研究针对该研究空白开展,旨在明确二者的功能关联,为阐明阅读障碍及纤毛病的发病机制提供新的理论支撑,为后续开发相关疾病的干预靶点提供研究基础。
2. 文献综述解析
本研究文献综述部分按照两个候选基因的功能重叠维度展开评述,首先梳理阅读障碍候选基因的研究进展,再分别阐述DYX1C1与DCDC2在神经元迁移、纤毛功能调控中的作用,最后引入二者潜在的共同互作蛋白中心体P4.1相关蛋白(CPAP)的已有研究结论。
现有研究的关键支持结论包括:啮齿类基因敲低模型与体外实验均证实DYX1C1与DCDC2参与神经元迁移,与尸检发现的阅读障碍患者大脑神经元迁移异常的表型高度一致;DYX1C1突变可导致原发性纤毛运动障碍,DCDC2功能缺失突变可引发肾单位肾痨相关纤毛病、遗传性听力损失等多种纤毛相关疾病,二者在高纤毛表达的组织中均呈现显著表达上调。现有研究的技术方法优势在于,斑马鱼模型已被广泛用于纤毛病基因的功能验证,单个基因敲低即可稳定再现纤毛病相关表型,免疫共沉淀、免疫荧光等技术可稳定验证蛋白相互作用与亚细胞定位特征。现有研究的局限性在于,仅针对单个基因的功能进行了初步解析,未探讨两个功能高度重叠的候选基因之间的相互作用,也未明确二者调控纤毛功能的共同分子通路。
本研究的创新价值在于首次证实DYX1C1、DCDC2与CPAP存在蛋白水平的相互作用,同时在斑马鱼模型中验证了二者的协同遗传效应,还发现了二者在特定细胞类型中的相互转录调控,填补了领域内关于这两个阅读障碍候选基因功能关联的研究空白,为后续解析纤毛功能调控的分子网络提供了新的研究方向。
3. 研究思路总结与详细解析
本研究的核心目标是揭示阅读障碍候选基因DYX1C1与DCDC2的物理及功能相互作用,核心科学问题是二者是否通过共同的互作蛋白参与纤毛功能调控,技术路线遵循“蛋白互作验证→亚细胞共定位分析→体内遗传互作验证→转录调控分析”的逻辑闭环,覆盖体外细胞模型、脑类器官模型与体内斑马鱼模型,研究结论的可靠性较高。
3.1 蛋白相互作用验证
实验目的为验证DYX1C1、DCDC2与CPAP的内源性及外源性蛋白相互作用,并明确DYX1C1介导互作的核心结构域。方法细节为采用HeLa细胞、15天龄人诱导多能干细胞来源的脑类器官作为实验模型,通过免疫共沉淀实验检测内源性蛋白互作;采用四环素诱导表达CPAP-绿色荧光蛋白(GFP)的人永生化视网膜色素上皮细胞(hTERT-RPE1)稳定细胞系,转染携带V5标签的DYX1C1、DCDC2及DYX1C1结构域缺失突变体质粒,通过GFP-Trap下拉实验检测外源性互作。
结果解读为免疫共沉淀的蛋白免疫印迹结果显示,HeLa细胞中内源性DYX1C1、DCDC2均可与CPAP发生相互作用;15天龄脑类器官中也验证了DYX1C1与CPAP的内源性互作。结构域缺失实验显示,仅当DYX1C1的p23结构域缺失时,其与CPAP的互作完全消失,证实p23结构域是二者互作的核心介导区域。
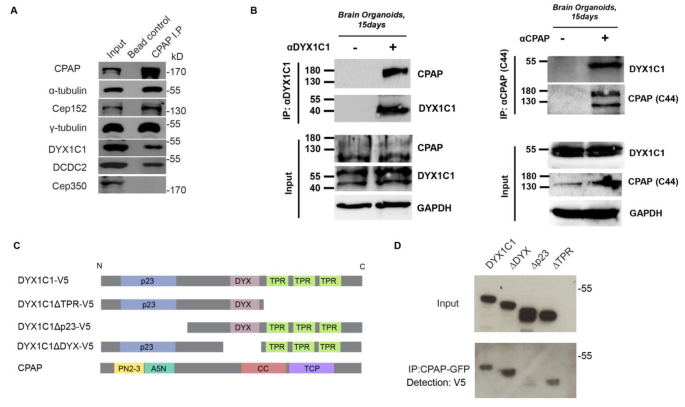
实验所用关键产品包括Proteintech的DYX1C1抗体(货号14522-1-AP)、Thermo Fisher的GFP-Trap下拉试剂盒、Invitrogen的V5-辣根过氧化物酶(HRP)抗体,其余实验试剂为分子生物学常规试剂。
3.2 亚细胞共定位分析
实验目的为明确DYX1C1、DCDC2与CPAP的亚细胞共定位特征及细胞周期依赖性。方法细节为采用hTERT-RPE1细胞作为实验模型,通过免疫荧光染色结合共聚焦显微镜观察内源性蛋白的亚细胞定位。
结果解读为免疫荧光结果显示,正常血清培养的hTERT-RPE1细胞中,DYX1C1与CPAP在中心体位置共定位;DCDC2与CPAP的共定位具有细胞周期依赖性,胞质分裂期二者无共定位,而中期时DCDC2定位于中心体和纺锤丝,与CPAP存在共定位。
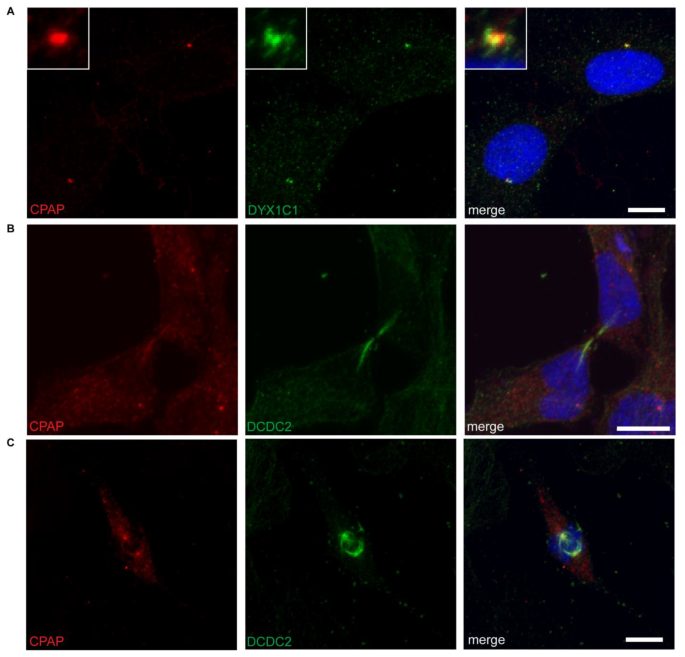
实验所用关键产品包括Sigma的DYX1C1抗体(货号SAB4200128)、Abcam的DCDC2抗体(货号ab157186)、Nikon A1R共聚焦显微镜。
3.3 斑马鱼体内遗传互作验证
实验目的为验证dyx1c1与dcdc2b在体内的遗传互作效应。方法细节为采用AB品系斑马鱼作为体内模型,选择20μM的dyx1c1吗啉代寡核苷酸(MO)和100μM的dcdc2b MO作为亚表型剂量,该剂量单独注射无明显纤毛病表型,将两种MO共同注射到1细胞期斑马鱼胚胎中,以注射标准对照MO的胚胎为对照,受精后2天观察表型,每组实验样本量为100枚胚胎。
结果解读为单独注射亚剂量dyx1c1 MO或dcdc2b MO的胚胎中,95%以上个体表型与野生型一致;而共同注射两种MO的胚胎中,60%的个体出现严重的躯体弯曲等纤毛病表型(n=100),提示二者存在协同遗传互作,共同调控纤毛功能。
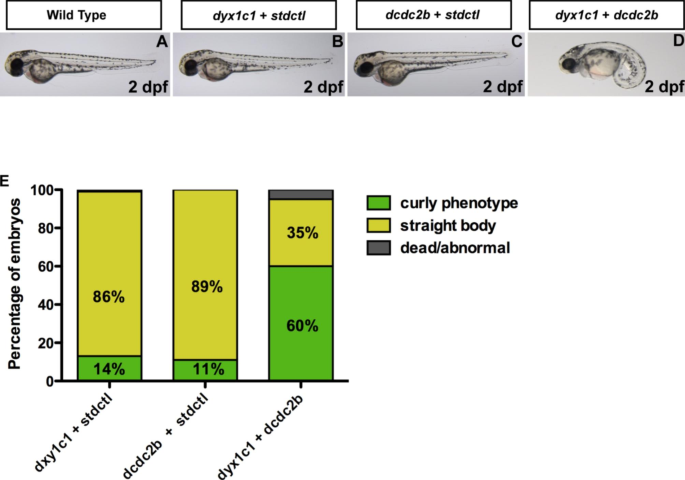
实验所用吗啉代寡核苷酸购自Gene Tools公司,其余为斑马鱼养殖常规试剂。
3.4 转录调控关系分析
实验目的为明确DYX1C1与DCDC2之间是否存在转录水平的调控关系。方法细节为采用hTERT-RPE1细胞和斑马鱼胚胎作为模型,通过小干扰RNA(siRNA)敲低hTERT-RPE1细胞中的DYX1C1或DCDC2,通过MO敲低斑马鱼胚胎中的dyx1c1,采用定量实时聚合酶链反应(qRT-PCR)检测靶基因的表达水平,每个实验设置3次生物学重复,采用t检验进行统计学分析。
结果解读为hTERT-RPE1细胞中,敲低DYX1C1可使DCDC2的表达水平显著下调(P<0.05,n=3),敲低DCDC2也可使DYX1C1的表达水平显著下调(P<0.05,n=3);而斑马鱼dyx1c1敲低胚胎中,受精后1天和2天的dcdc2b表达水平均无显著变化(P分别为0.2597和0.4521,n=3),提示二者的转录调控具有细胞类型特异性。
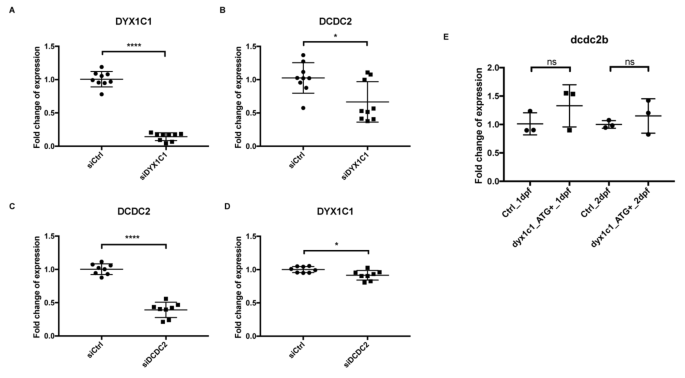
实验所用siRNA购自Dharmacon公司,qRT-PCR试剂购自Roche和Thermo Fisher Scientific公司。
4. Biomarker研究及发现成果
本研究未涉及临床诊断或预后相关生物标志物的筛选,主要围绕纤毛功能调控相关的功能分子互作展开,相关研究成果为后续开发阅读障碍及纤毛病的分子标志物提供了新的候选靶点。
本研究筛选到的核心功能互作模块为DYX1C1-DCDC2-CPAP蛋白复合物,其中DYX1C1通过p23结构域介导与CPAP的结合,二者的相互作用是调控纤毛功能的关键分子事件。该模块的验证过程覆盖了细胞系、脑类器官和斑马鱼多个模型,结果一致性较高。目前暂无该模块作为生物标志物的敏感性、特异性相关临床数据,后续可通过临床队列研究进一步验证该复合物组分的表达异常是否可作为阅读障碍或纤毛病的早期筛查标志物。
推测:DYX1C1和DCDC2的表达水平及二者的互作状态可作为纤毛功能异常的潜在分子标志物,为神经发育疾病的诊断提供新的方向,后续可扩大临床样本量开展相关验证研究。