1. 领域背景与文献引入
文献英文标题:Overexpression of ephrinB2 in dental pulp stem cells promotes in vitro capillary-like cord formation and in vivo vascularization in a 3D bioprinted hydrogel;发表期刊:BMC Medical Materials;影响因子:未公开;研究领域:组织工程与再生医学(工程化组织血管化方向)
组织工程与再生医学领域中,工程化组织构建体的快速血管化是实现临床转化的核心瓶颈。领域共识:宿主血管向植入物内的生长速率仅为5-17μm/h,自发血管化过程需数周时间,易导致构建体内细胞因长期缺血死亡、组织坏死,严重限制了工程化组织的临床应用。预血管化策略通过在植入前于构建体内构建成熟的血管网络,成为解决该问题的最具潜力方向之一,其核心是将内皮细胞(ECs)与间质干细胞(MSCs)共培养,MSCs可分化为周样细胞参与血管的稳定与成熟。牙髓干细胞(DPSCs)作为易从废弃牙齿中获取的MSCs亚型,已被证实可通过旁分泌血管生成因子或直接细胞接触参与血管形成,但3D共培养体系中,ephrinB2/EphB4直接接触信号通路对血管样结构组装的调控机制尚不明确,这是当前领域的研究空白。本研究针对该问题,利用3D生物打印明胶甲基丙烯酸酯(GelMA)水凝胶模型,系统探究DPSCs中ephrinB2对体外毛细血管样索形成及体内血管化的调控作用,为工程化组织的预血管化策略提供新的分子靶点与实验依据。
2. 文献综述解析
作者对领域内现有研究的分类维度主要包括:血管化策略的细胞组合类型(ECs单独培养、ECs与成纤维细胞共培养、ECs与MSCs共培养)、细胞间信号传导方式(旁分泌信号、直接接触的juxtracrine信号)、培养体系的空间维度(2D平面培养、3D三维培养)。
现有研究显示,ECs单独在胶原、纤维蛋白等部分水凝胶中可自发形成血管样网络,但在GelMA水凝胶中无法独立完成该过程,需MSCs的辅助作用;DPSCs作为MSCs的亚型,可通过旁分泌血管内皮生长因子(VEGF)等细胞因子促进ECs的迁移与增殖,同时可分化为表达周样细胞标志物的细胞,包裹在血管样结构外层以维持血管稳定;2D培养体系中,ephrinB2信号通路已被证实可调控DPSCs与ECs的血管样网络形成,敲低DPSCs中ephrinB2会抑制血管样结构组装,过表达则促进该过程,但3D共培养体系中尤其是3D生物打印模型中,该信号通路的具体作用机制尚未明确。现有研究的局限性在于缺乏对3D环境中细胞直接接触信号的深入探究,且未结合临床转化潜力更高的3D生物打印技术开展实验。
本研究的创新价值在于,首次在3D生物打印GelMA水凝胶模型中明确证实,DPSCs与ECs的直接接触是血管样索形成的必要条件,而非仅依赖旁分泌信号;同时系统阐明了DPSCs中ephrinB2信号通路对体外血管样索形成及体内血管化的调控作用,为工程化组织预血管化策略的优化提供了新的分子靶点,弥补了3D体系中该信号通路研究的空白。
3. 研究思路总结与详细解析
本研究的整体框架为:以“明确DPSCs中ephrinB2对3D生物打印水凝胶血管化的调控作用”为研究目标,围绕“DPSCs与HUVECs的直接接触信号是否为3D血管样结构形成的关键”这一核心科学问题,采用“细胞鉴定→模型构建→条件优化→信号调控→体内验证”的闭环技术路线,通过体外细胞实验与体内动物实验系统验证ephrinB2的调控功能。
3.1 细胞培养与鉴定
实验目的:获取并鉴定符合实验标准的DPSCs与人脐静脉内皮细胞(HUVECs),为后续3D模型构建提供标准化细胞工具。
方法细节:从健康志愿者(18-25岁)拔除的第三磨牙中分离牙髓组织,采用3mg/ml胶原酶I与4mg/ml dispase联合消化1小时,获取的细胞使用含20%胎牛血清的α-MEM培养基培养,传代3-8代用于实验;通过流式细胞术检测MSCs标志物(CD73、CD90、CD105)与造血细胞标志物(CD45)的表达,同时验证其成骨、成脂、成神经多向分化潜能;HUVECs购自ScienCell公司,使用内皮细胞培养基培养,传代6代以内用于实验。
结果解读:DPSCs呈成纤维细胞样形态,流式细胞术结果显示其CD73阳性率为99.77±0.32%(n=3)、CD90为98.7±1.65%(n=3)、CD105为99.73±0.21%(n=3),CD45阳性率仅为0.10±0.05%(n=3),且具备多向分化潜能,符合MSCs的鉴定标准;HUVECs保持典型的内皮细胞形态与功能,适合用于血管形成实验。
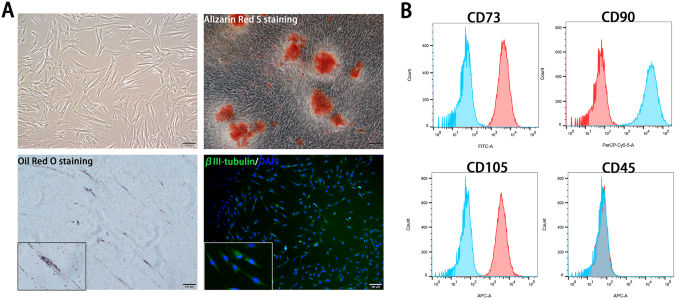
产品关联:实验所用关键产品:Gibco的胶原酶I、dispase、α-MEM培养基、胎牛血清;ScienCell的HUVECs与内皮细胞培养基;Proteintech的CD系列流式抗体。
3.2 3D生物打印GelMA水凝胶构建与体外血管样索观察
实验目的:构建DPSCs与HUVECs共培养的3D生物打印模型,明确DPSCs对HUVECs形成血管样索的作用机制。
方法细节:制备5%(w/v)GelMA30(功能化程度30%)生物墨水,分别加载单独HUVECs、HUVECs与DPSCs按1:3比例共培养的细胞悬液,使用Regenovo Bio-Architect® SR生物打印机打印为直径8mm、4层的圆柱形结构,经405nm紫外光交联40s;使用Leica STELLARIS 5共聚焦显微镜观察mCherry标记的HUVECs形成的血管样索,采用Image J软件分析分支点数量与索长度;通过免疫荧光染色检测CD31(HUVECs标志物)、SM22α与αSMA(周样细胞标志物)的表达。
结果解读:仅HUVECs与DPSCs直接共培养组形成了大量含管腔的血管样索,DPSCs紧密包裹在索的外层并表达SM22α与αSMA周样细胞标志物;单独HUVECs组或添加DPSCs条件培养基、共培养条件培养基的组别均未形成明显的血管样索,说明DPSCs与HUVECs的直接接触是血管样索形成的必要条件,旁分泌信号无法单独诱导该过程。
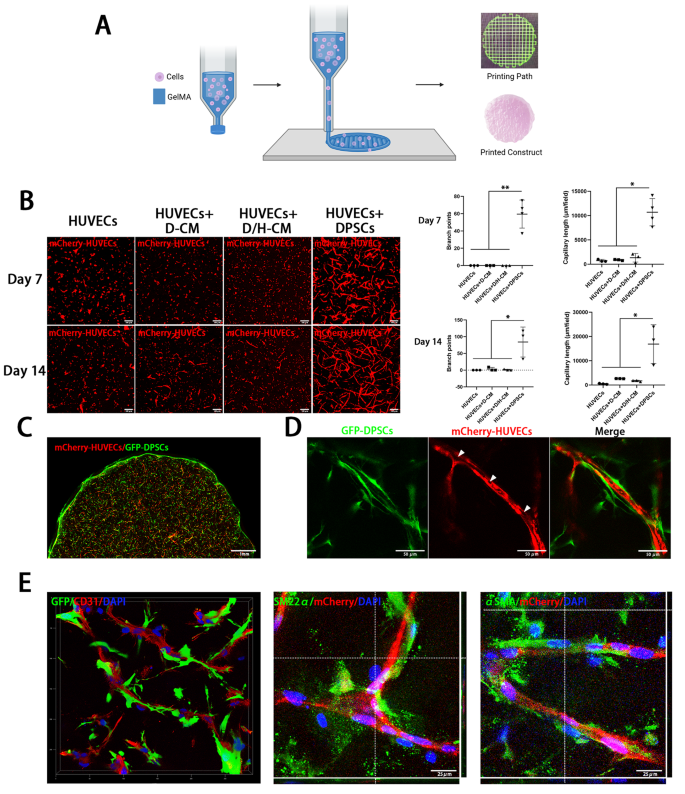
产品关联:实验所用关键产品:Engineering for Life的GelMA30;Regenovo的Bio-Architect® SR生物打印机;Leica的STELLARIS 5共聚焦显微镜;Proteintech的CD31、SM22α、αSMA抗体。
3.3 血管样索形成的条件优化
实验目的:确定促进3D生物打印水凝胶中血管样索形成的最佳DPSCs:HUVECs比例与GelMA功能化程度(DoF)。
方法细节:设置DPSCs:HUVECs比例为1:1、1:3、1:5三个组别,GelMA DoF为30%、60%、90%三个组别,共培养14天后,通过共聚焦显微镜观察血管样索形态,Image J分析分支点数量与索长度。
结果解读:DPSCs:HUVECs比例为1:3时,血管样索的分支点数量提升2倍以上,索长度提升3倍以上(n=3,P<0.01);GelMA DoF从30%提升至60%、90%时,血管样索的形成被显著抑制,分支点数量与索长度均明显降低,说明低DoF的GelMA水凝胶更有利于细胞的迁移与相互作用,进而促进血管样索的形成。

产品关联:文献未提及具体实验产品,领域常规使用Image J软件进行血管形态学定量分析。
3.4 ephrinB2信号通路的调控实验
实验目的:验证ephrinB2/EphB4信号通路对3D生物打印水凝胶中血管样索形成的调控作用。
方法细节:向共培养体系中添加100μM EphB4抑制肽TNYL-RAW以阻断ephrinB2/EphB4信号通路,同时设置添加对照肽SCR-WTL的对照组;通过慢病毒转染技术,分别敲低与过表达DPSCs中的ephrinB2,采用Western blot验证敲低(表达量降低约50%)与过表达(表达量提升约1.6倍)的效率;共培养14天后,观察血管样索的形成情况并定量分析。
结果解读:添加TNYL-RAW肽后,血管样索的长度降低30%,分支点数量降低52%(n=3,P<0.01);敲低DPSCs中ephrinB2后,血管样索的形成显著减少;过表达DPSCs中ephrinB2后,血管样索的分支点数量与长度均显著增加,说明ephrinB2信号通路是DPSCs促进HUVECs形成血管样索的关键调控因子。
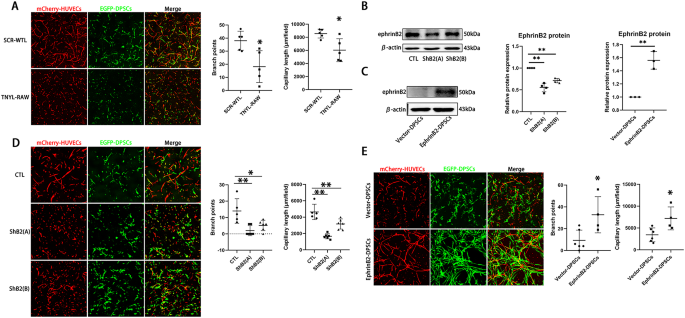
产品关联:实验所用关键产品:GeneCopoeia的慢病毒载体;Abcam的ephrinB2抗体;Tanon的凝胶成像系统;GL Biochem的EphB4抑制肽与对照肽。
3.5 体内血管化验证实验
实验目的:验证3D生物打印水凝胶在体内的血管化能力,以及DPSCs中ephrinB2过表达对体内血管化的促进作用。
方法细节:将体外培养7天的5组水凝胶构建体(空白GelMA组、仅DPSCs组、仅HUVECs组、DPSCs+HUVECs组、ephrinB2过表达DPSCs+HUVECs组)皮下植入SCID小鼠背部,每组4个移植样本;14天后处死小鼠,取出植入物进行HE染色与免疫组化染色(抗人CD31抗体),观察并统计血管数量。
结果解读:仅DPSCs+HUVECs组与ephrinB2过表达组的植入物中形成了含红细胞的成熟血管,其中ephrinB2过表达组的血管数量较野生型DPSCs组提升3倍以上(n=3,P<0.01),说明ephrinB2过表达可显著促进工程化组织构建体的体内血管化与血液灌注。
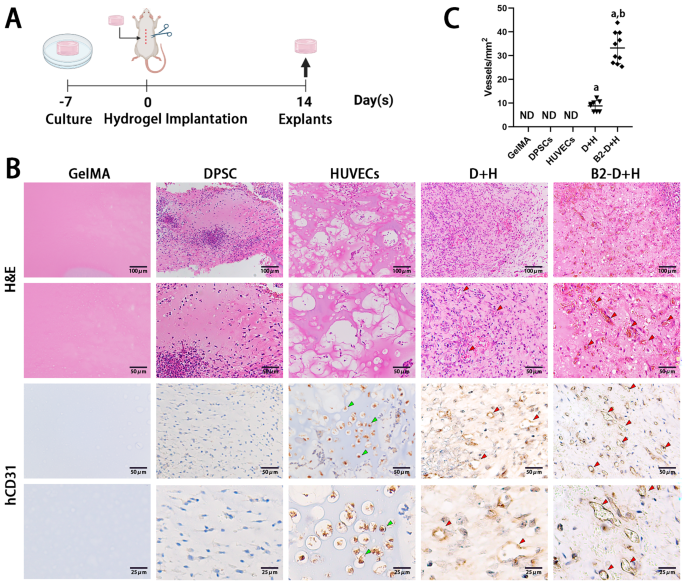
产品关联:实验所用关键产品:北京维通利华的SCID小鼠;Proteintech的抗人CD31单克隆抗体;武汉Servicebio的组织病理检测服务。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的Biomarker为牙髓干细胞(DPSCs)细胞膜表面的ephrinB2蛋白,其筛选与验证逻辑为:基于2D培养体系中ephrinB2调控DPSCs与ECs血管形成的研究基础,提出3D体系中该分子可能参与血管样索形成的假设→通过3D生物打印模型验证ephrinB2信号通路对体外血管样索形成的调控作用→通过体内动物实验验证ephrinB2过表达对体内血管化的促进作用,形成完整的“假设-体外验证-体内验证”逻辑链条。
研究过程详述
ephrinB2的来源为DPSCs的细胞膜,验证方法包括:采用Western blot技术定量检测DPSCs中ephrinB2的表达水平,明确敲低与过表达的效率;通过免疫荧光染色定位ephrinB2在细胞间的表达与分布;通过功能实验,分别在体外3D模型与体内动物模型中,验证ephrinB2表达水平变化对血管样索形成、血管数量的影响。特异性与敏感性方面,研究显示仅在DPSCs与HUVECs直接共培养的体系中,ephrinB2信号通路可有效激活并调控血管化过程,过表达ephrinB2可特异性提升体内血管数量,但未提供ROC曲线、敏感性、特异性的具体数据。
核心成果提炼
该Biomarker的功能关联为:DPSCs中的ephrinB2通过与HUVECs表面的EphB4受体结合,激活直接接触的juxtracrine信号通路,促进HUVECs在3D生物打印水凝胶中形成含管腔的毛细血管样索,并显著提升工程化组织构建体在体内的血管化效率与血液灌注。其创新性在于,首次在3D生物打印GelMA水凝胶模型中明确证实ephrinB2对DPSCs-HUVECs共培养体系血管化的调控作用,为工程化组织的预血管化策略提供了新的分子靶点。统计学结果显示,ephrinB2过表达组的体内血管数量较野生型DPSCs组提升3倍以上(n=3,P<0.01),差异具有统计学意义。