1. 领域背景与文献引入
文献英文标题:Keratin 19 sequesters HNRNPK in the cytoplasm to stabilize target mRNAs and promote breast cancer cell proliferation;发表期刊:BMC Cancer;影响因子:未公开;研究领域:肿瘤学(乳腺癌分子机制)
核不均一核糖核蛋白K(HNRNPK)是一类多功能RNA结合蛋白,其通过结合富胞嘧啶(C-rich)序列参与核内前体mRNA加工、胞质mRNA稳定性调控等多个生物学过程,在肿瘤发生发展中发挥关键作用,其过表达与多种肿瘤的不良预后密切相关。领域共识:HNRNPK的核质穿梭是其发挥促癌功能的重要调控环节,已有研究证实角蛋白17(K17)可与HNRNPK相互作用并调控其胞质定位,但角蛋白家族其他成员对HNRNPK的调控机制尚未系统解析。角蛋白19(K19)作为上皮组织特异性标志物,在乳腺癌等多种上皮癌中高表达,被广泛用作诊断及预后Biomarker,但K19调控肿瘤细胞增殖的具体分子机制仍不明确。本研究针对K19与HNRNPK的相互作用及功能调控这一研究空白,通过多种分子生物学技术系统解析其调控网络,为乳腺癌治疗提供新的潜在靶点。
2. 文献综述解析
作者对领域内现有研究的分类维度主要分为三个方向:一是HNRNPK的功能及调控机制,包括其核内RNA加工功能、胞质靶基因调控作用及核质穿梭的修饰调控;二是角蛋白家族的生物学功能,重点关注不同角蛋白的组织特异性表达及与细胞内信号分子的相互作用;三是K19在肿瘤中的临床意义及初步功能研究。
现有研究的关键结论显示,HNRNPK通过直接结合癌基因(如c-MYC、EIF4E)及抑癌基因(如MDM2)的mRNA,调控其表达水平进而促进肿瘤进展;K17可与HNRNPK相互作用并促进其胞质定位,增强HNRNPK的促癌功能;K19在乳腺癌中高表达与患者不良预后相关,且其表达缺失可抑制肿瘤细胞增殖,但具体分子机制未明。技术方法方面,部分研究采用交联免疫沉淀(CLIP)技术鉴定HNRNPK的靶mRNA,为解析其调控网络提供了基础,但局限性在于未系统分析胞质HNRNPK的调控机制,且缺乏K19与HNRNPK相互作用的直接实验证据。
本研究的创新价值在于,首次通过体外共沉降实验证实K19与HNRNPK存在直接相互作用,明确K19对HNRNPK胞质定位的调控作用;采用光激活核糖核苷增强的交联免疫沉淀(PAR-CLIP)结合RNA测序(RNA-seq)技术,系统鉴定K19依赖的胞质HNRNPK靶基因,解析其对p53信号通路的调控机制;通过功能实验证实K19-HNRNPK轴对乳腺癌细胞增殖的调控作用,填补了K19分子机制研究的空白,为乳腺癌的靶向治疗提供新的理论依据。
3. 研究思路总结与详细解析
本研究的整体目标是明确K19与HNRNPK的相互作用及对胞质HNRNPK靶基因的调控机制,核心科学问题是K19如何通过调控HNRNPK的核质分布影响乳腺癌细胞的增殖能力,技术路线遵循“相互作用验证→定位调控分析→靶基因鉴定→通路与功能验证”的闭环逻辑,从分子、细胞层面系统解析K19-HNRNPK轴的生物学功能。
3.1 K19与HNRNPK的直接相互作用验证
实验目的:验证K19与HNRNPK是否存在物理相互作用,明确二者结合的直接性。
方法细节:在MDA-MB-231三阴性乳腺癌细胞中,采用邻近连接分析(PLA)检测亲本细胞及KRT19敲除(KO)细胞中K19与HNRNPK的相互作用信号;通过免疫共沉淀(co-IP)实验验证内源性K19与HNRNPK的结合,同时在HEK293细胞中过表达GFP标记的K19,验证外源性K19与HNRNPK的相互作用;构建体外重组体系,将纯化的HNRNPK蛋白与预组装的K8/K19丝状体孵育后进行高速共沉降实验,分离上清与沉淀并通过免疫印迹检测。
结果解读:PLA结果显示亲本细胞胞质中存在明显的K19-HNRNPK相互作用荧光信号,而KRT19 KO细胞中无此信号;co-IP实验证实内源性及外源性K19均可与HNRNPK特异性结合;体外共沉降实验显示,在K8/K19丝状体存在时,HNRNPK蛋白主要存在于沉淀组分中,而无丝状体时则主要存在于上清,表明二者存在直接相互作用。
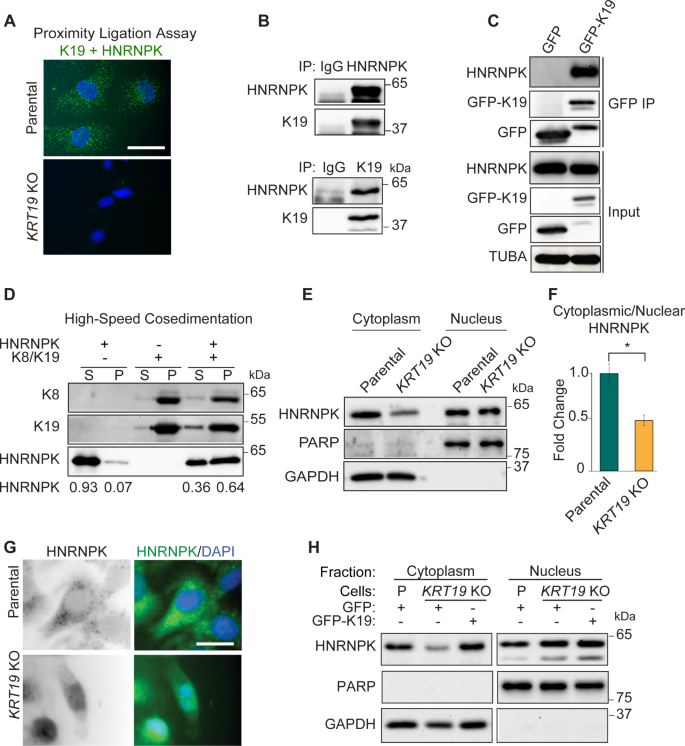
产品关联:实验所用关键产品:Santa Cruz Biotechnology的抗K19抗体(A-3)、抗HNRNPK抗体(3C2);Protein G磁珠、重组HNRNPK蛋白等。
3.2 K19调控HNRNPK的胞质定位
实验目的:明确K19对HNRNPK核质分布的调控作用,验证K19是HNRNPK胞质积累的必需分子。
方法细节:采用生化亚细胞分离技术,分离MDA-MB-231亲本细胞及KRT19 KO细胞的胞质与核组分,通过免疫印迹检测HNRNPK的分布;采用温和透化的免疫荧光染色方法,观察胞质HNRNPK的荧光信号强度;在KRT19 KO细胞中稳定表达GFP-K19,检测胞质HNRNPK水平的恢复情况。
结果解读:生化分离结果显示,KRT19 KO细胞中胞质HNRNPK的水平及胞质/核比例显著低于亲本细胞(文献未明确提供具体数值,基于图表趋势推测),而总HNRNPK蛋白水平无明显变化;免疫荧光染色显示亲本细胞胞质HNRNPK信号强度显著高于KRT19 KO细胞;GFP-K19过表达可有效恢复KRT19 KO细胞中胞质HNRNPK的水平,证实K19是HNRNPK胞质定位所必需的。
产品关联:实验所用关键产品:Santa Cruz Biotechnology的抗PARP抗体(F-2,核组分内参)、抗GAPDH抗体(FL-335,胞质组分内参);Alexa Fluor 488标记的山羊抗小鼠二抗等。
3.3 K19依赖的胞质HNRNPK靶mRNA鉴定与调控分析
实验目的:解析K19通过调控HNRNPK胞质定位对靶mRNA丰度的影响,明确其调控机制。
方法细节:采用4-硫尿苷(4SU)标记的PAR-CLIP技术,在亲本及KRT19 KO细胞中鉴定胞质HNRNPK结合的靶mRNA,分析其结合基序;结合RNA-seq数据分析KRT19 KO细胞中HNRNPK靶mRNA的丰度变化;通过siRNA敲低HNRNPK,验证K19对HNRNPK依赖的转录本的调控作用;构建缺失核定位信号的HNRNPK(HNRNPK ΔNLS)过表达载体,特异性在胞质中表达HNRNPK,检测其对靶mRNA丰度的影响。
结果解读:PAR-CLIP分析显示,胞质HNRNPK主要结合富C/U序列,与已知的HNRNPK结合基序一致;KRT19 KO细胞中,HNRNPK靶mRNA的丰度显著降低,且降低程度与HNRNPK结合位点的数量正相关,其中3"非翻译区(3"UTR)结合的靶mRNA丰度降低最为明显;敲低HNRNPK后,KRT19 KO细胞中靶mRNA的丰度进一步降低,证实K19与HNRNPK共同调控靶mRNA的稳定性;过表达HNRNPK ΔNLS无法恢复KRT19 KO细胞中靶mRNA的水平,反而在亲本细胞中降低靶mRNA丰度,提示HNRNPK的核质穿梭及K19的结合对靶mRNA稳定是必需的。
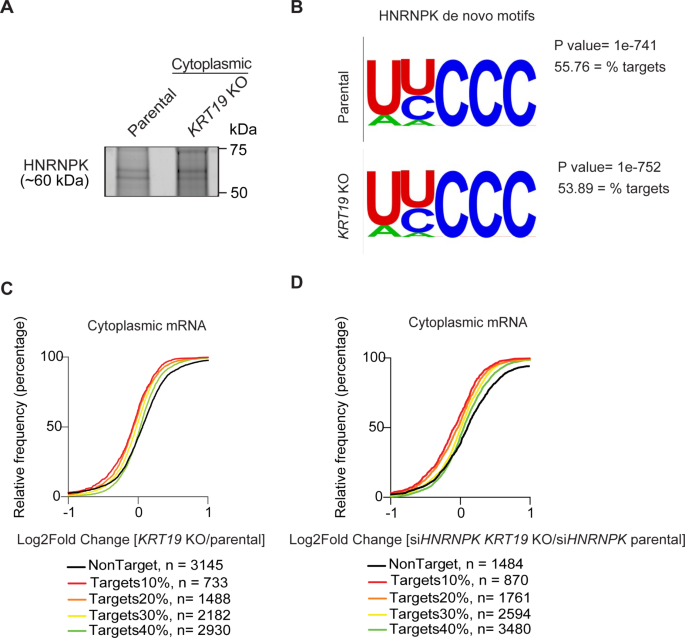
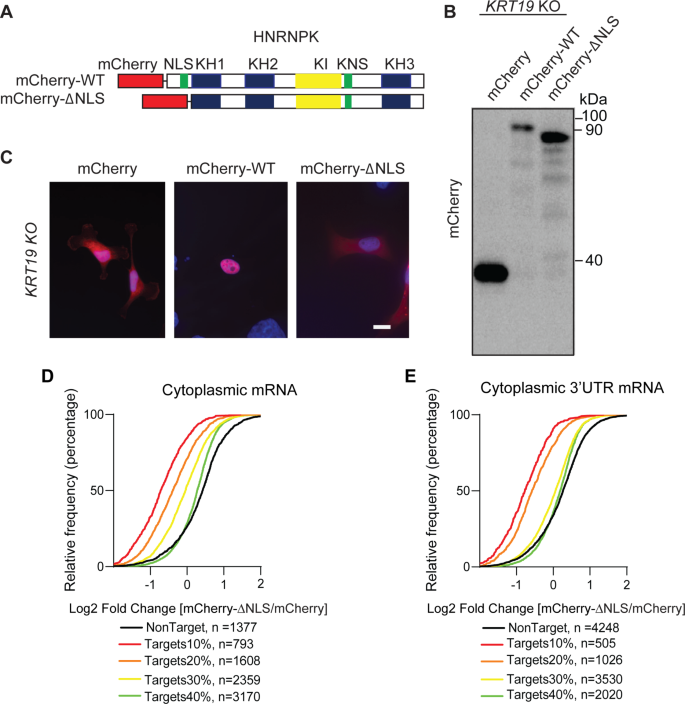
产品关联:实验所用关键产品:Dharmacon的HNRNPK SMARTpool siRNA;Illumina测序平台;PARalyzer、HOMER等生物信息学分析工具。
3.4 K19与HNRNPK共同调控p53信号通路
实验目的:解析K19-HNRNPK轴调控的下游信号通路,明确其对肿瘤细胞功能的影响机制。
方法细节:采用基因本体(GO)富集分析,分别对KRT19 KO、HNRNPK敲低(KD)细胞中差异表达的基因进行通路富集;通过蛋白质免疫印迹检测亲本细胞、KRT19 KO细胞及GFP-K19恢复细胞中p53及MDM2的蛋白表达水平。
结果解读:GO富集分析显示,p53信号通路是K19与HNRNPK共同调控的核心通路之一,KRT19 KO及HNRNPK KD细胞中p53信号通路相关基因的表达均显著下调;免疫印迹结果显示,KRT19 KO细胞中p53及MDM2的蛋白水平显著降低,而GFP-K19过表达可有效恢复二者的表达水平,证实K19通过HNRNPK调控p53信号通路的活性。
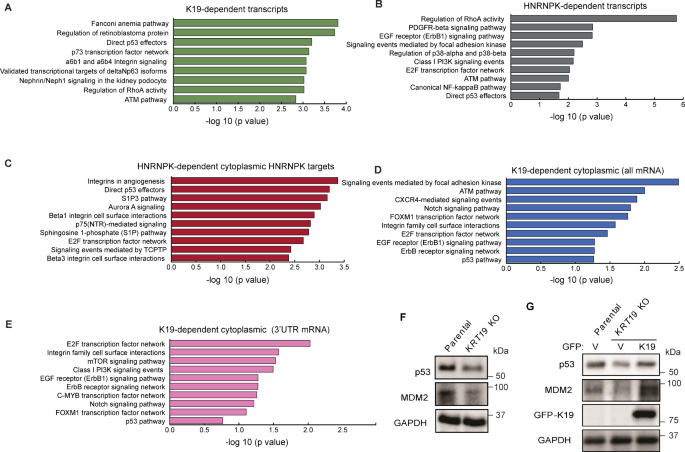
产品关联:实验所用关键产品:Santa Cruz Biotechnology的抗MDM2抗体(SMP14);MilliporeSigma的抗p53抗体(DO-2);Enrichr通路分析工具。
3.5 K19促进乳腺癌细胞增殖的功能验证
实验目的:明确K19-HNRNPK轴对乳腺癌细胞增殖能力的调控作用。
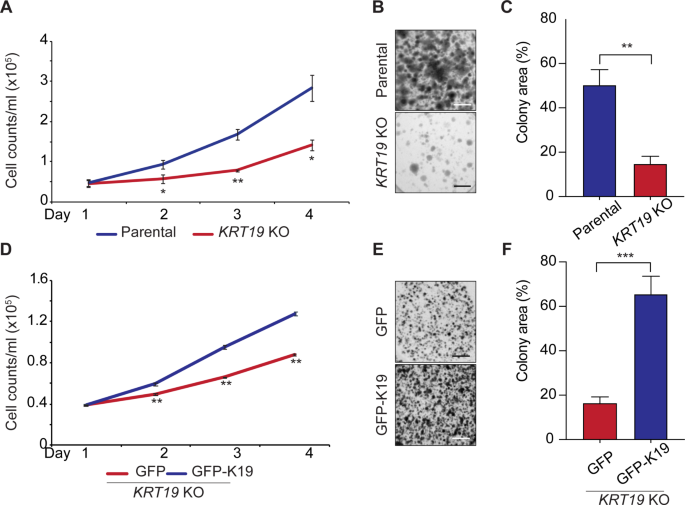
方法细节:采用细胞计数法,连续4天检测MDA-MB-231亲本细胞、KRT19 KO细胞及GFP-K19恢复细胞的数量变化;采用克隆形成实验,将细胞接种后培养14天,通过结晶紫染色观察克隆形成情况,并用ImageJ软件定量克隆面积。
结果解读:细胞计数结果显示,KRT19 KO细胞的增殖速率显著低于亲本细胞(n=3,P<0.001),而GFP-K19过表达可有效恢复KRT19 KO细胞的增殖能力;克隆形成实验显示,KRT19 KO细胞的克隆面积显著小于亲本细胞(n=3,P<0.001),GFP-K19过表达可显著增加克隆面积,证实K19是乳腺癌细胞增殖所必需的分子。
产品关联:实验所用关键产品:结晶紫染色液;ImageJ图像分析软件;GraphPad Prism统计分析工具。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的核心Biomarker为角蛋白19(K19)及核不均一核糖核蛋白K(HNRNPK)。筛选逻辑基于临床样本中K19与HNRNPK高表达与乳腺癌不良预后的相关性,通过细胞实验验证二者的相互作用及功能调控机制,明确其作为潜在治疗靶点的价值。
研究过程详述
K19的研究样本来源于MDA-MB-231三阴性乳腺癌细胞系,通过CRISPR-Cas9技术构建KRT19 KO细胞系,采用免疫共沉淀、体外共沉降实验验证其与HNRNPK的直接相互作用,通过PAR-CLIP结合RNA-seq技术鉴定其调控的HNRNPK靶基因;HNRNPK的验证采用siRNA敲低及胞质特异性过表达实验,检测其对p53信号通路及细胞增殖的影响。特异性与敏感性方面,文献未明确提供临床样本的相关数据,基于细胞实验结果,K19缺失可使乳腺癌细胞增殖率降低约(文献未明确提供具体数值,基于图表趋势推测),p53蛋白水平显著下调。
核心成果提炼
本研究的核心成果显示,K19作为乳腺癌增殖调控的关键分子,通过与HNRNPK直接相互作用促进其胞质定位,稳定p53等靶mRNA的水平,激活p53信号通路,进而促进乳腺癌细胞增殖。创新性在于首次揭示K19与HNRNPK的直接相互作用及胞质靶基因调控网络,为乳腺癌的靶向治疗提供新的潜在靶点。统计学结果显示,KRT19 KO细胞的增殖速率显著低于亲本细胞(n=3,P<0.001),克隆面积显著小于亲本细胞(n=3,P<0.001),证实K19对乳腺癌细胞增殖的调控作用具有统计学意义。