1. 领域背景与文献引入
文献英文标题:D-MEKK1, the Drosophila orthologue of mammalian MEKK4/MTK1, and Hemipterous/D-MKK7 mediate the activation of D-JNK by cadmium and arsenite in Schneider cells;发表期刊:BMC Cell Biology;影响因子:未公开;研究领域:细胞信号转导(重金属诱导的c-Jun氨基末端激酶通路激活)
c-Jun氨基末端激酶(JNK)属于丝裂原活化蛋白激酶(MAPK)家族,在胚胎发育、细胞应激反应(如氧化应激、重金属暴露)中发挥关键作用。领域共识:哺乳动物中JNK通路的上游调控存在高度冗余,包括至少13种JNK激酶激酶(JNKKK)和2种JNK激酶(JNKK:MKK4、MKK7),这导致难以明确特定应激源(如重金属)激活JNK的具体信号模块。镉、亚砷酸钠等重金属是JNK的强效激活剂,现有研究表明其激活依赖氧化应激,但哺乳动物系统中关于上游激酶的作用存在矛盾报道,例如部分研究认为MKK4和MKK7均参与镉诱导的JNK激活,而另一些研究仅支持MKK7的作用;JNKKK方面,MEKK家族、ASK1均被报道参与,但结果不一致。
为解决哺乳动物系统的冗余问题,作者采用基因冗余度更低的果蝇Schneider(S2)细胞模型,结合RNA干扰(RNAi)技术,系统筛选镉和亚砷酸钠激活D-JNK的上游调控因子,旨在明确进化保守的重金属诱导JNK激活的核心信号通路,为哺乳动物相关研究提供简化模型与进化依据。
2. 文献综述解析
作者的综述逻辑围绕“JNK通路的进化保守性与哺乳动物系统研究困境”展开,先介绍MAPK家族尤其是JNK的功能与上游调控网络,再聚焦重金属激活JNK的机制争议,最后提出果蝇模型的优势。
哺乳动物中JNK通路参与多种生理病理过程,上游调控涉及小G蛋白、多类JNKKK和JNKK,其中JNKKK的多样性是通路特异性调控的关键,但也导致了研究复杂性。镉、亚砷酸钠等重金属通过诱导氧化应激激活JNK,然而关于具体的JNKK-JNKKK模块,现有研究存在矛盾:在JNKK层面,部分研究认为MKK4和MKK7共同介导镉诱导的JNK激活,另一部分研究则仅发现MKK7的作用;在JNKKK层面,MEKK家族成员、ASK1均被报道参与,但不同研究的实验体系与结果存在差异,甚至有研究提出砷酸盐通过抑制JNK磷酸酶而非激活上游激酶来激活JNK。这些矛盾主要源于哺乳动物系统的基因冗余与实验体系差异,缺乏简化模型的验证。
本研究的创新点在于利用果蝇S2细胞的简化信号通路系统(仅含1种JNK、2种JNKK、4种核心JNKKK),结合RNAi高通量敲减技术,系统排查上游调控因子,首次明确了D-MEKK1(哺乳动物MEKK4/MTK1的同源物)和D-MKK7是镉和亚砷酸钠激活D-JNK的必需上游激酶,解决了哺乳动物系统中因冗余导致的研究矛盾,同时通过进化分析验证了该信号模块的保守性,为理解重金属诱导的细胞应激反应的进化起源提供了证据。
3. 研究思路总结与详细解析
整体研究框架为“模型验证→机制探究→因子筛选→进化分析”:首先验证镉和亚砷酸钠可激活果蝇S2细胞中的MAP激酶且依赖氧化应激;其次通过RNAi分别筛选JNKK和JNKKK中调控D-JNK激活的关键因子;随后排查小G蛋白的潜在作用;最后通过进化分析明确果蝇激酶与哺乳动物同源物的保守性。核心科学问题是明确重金属诱导D-JNK激活的上游核心信号模块,技术路线遵循“假设-验证-结论”的闭环逻辑,即假设果蝇中存在进化保守的重金属激活JNK的激酶模块,通过RNAi敲减验证每个上游因子的作用,最终确定核心模块。
3.1 重金属对果蝇MAP激酶的激活及毒性验证
实验目的:验证镉和亚砷酸钠能否激活果蝇S2细胞中的D-JNK、D-p38、D-ERK,并确定适合后续实验的低毒处理剂量。方法细节:将4×10^6个S2细胞接种于6孔板,培养2天后分别用不同浓度的氯化镉(10μM、100μM、200μM)和亚砷酸钠(50μM、200μM)处理不同时间(0.5h、1h、2h、4h),采用蛋白免疫印迹(WB)检测磷酸化形式的D-JNK、D-p38、D-ERK;用CellTiter-Blue™ Reagent检测处理24h后的细胞活力。结果解读:图1显示镉和亚砷酸钠以剂量和时间依赖的方式诱导三种MAP激酶的磷酸化,处理2h时激活水平达到峰值;图2显示100μM氯化镉处理24h后细胞存活率约60%(n=3,P<0.05,文献未明确提供具体数值,基于图表趋势推测),200μM亚砷酸钠处理24h后细胞存活率约45%(n=3,P<0.05,文献未明确提供具体数值,基于图表趋势推测);图3显示低至50μM的重金属即可显著激活三种MAP激酶,后续实验选择200μM处理2h以保证激活效率与细胞活力的平衡。产品关联:实验所用关键产品:Cell Signaling Technology的磷酸化JNK、p38、ERK抗体,Santa Cruz Biotechnology的JNK1抗体,Promega的CellTiter-Blue™ Reagent。
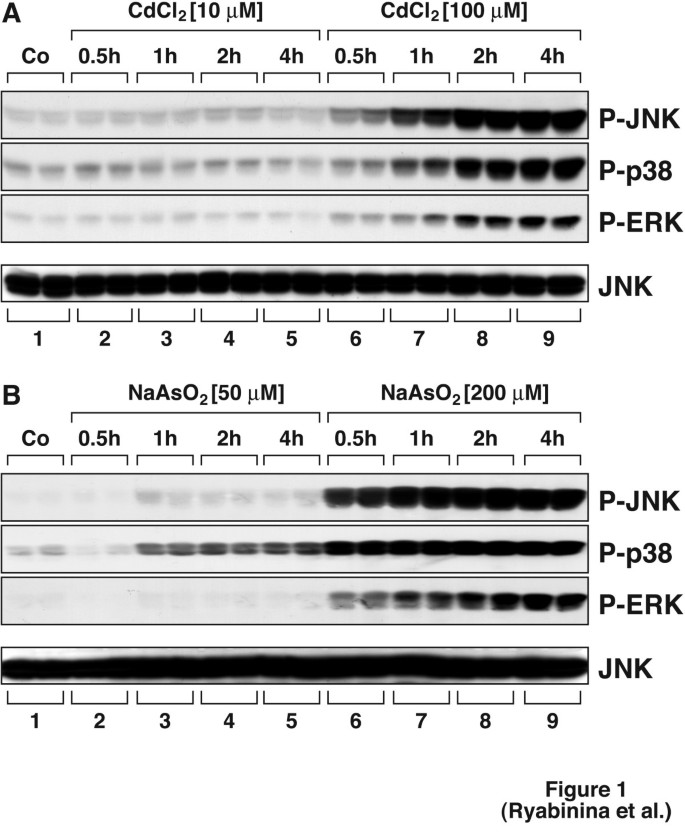
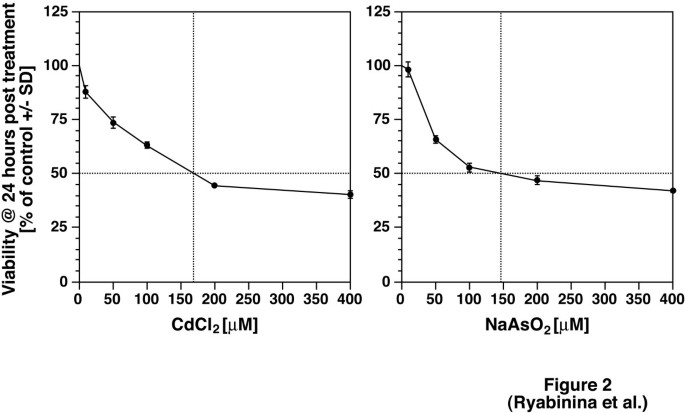
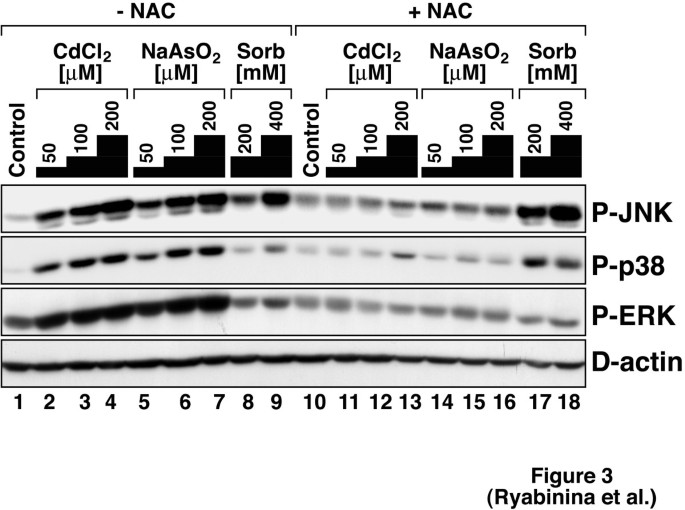
3.2 重金属激活MAP激酶依赖氧化应激的验证
实验目的:验证镉和亚砷酸钠激活果蝇MAP激酶是否通过氧化应激介导。方法细节:S2细胞接种后,在处理前30分钟加入终浓度30mM的N-乙酰半胱氨酸(NAC,ROS清除剂)预处理,随后用200μM氯化镉、200μM亚砷酸钠或200mM山梨醇(高渗应激对照)处理,2h后检测磷酸化MAP激酶水平;同时用Trolox(维生素E衍生物,抗氧化剂)重复实验以验证结果。结果解读:图3显示NAC预处理完全抑制了镉和亚砷酸钠诱导的三种MAP激酶的磷酸化,而对山梨醇诱导的D-JNK激活无影响;Trolox预处理得到类似结果(未展示),说明重金属通过氧化应激激活果蝇MAP激酶,该机制与哺乳动物系统一致。产品关联:实验所用关键产品:Sigma-Aldrich的N-乙酰半胱氨酸、Trolox。
3.3 JNKK在重金属激活D-JNK中的作用解析
实验目的:明确D-MKK4和D-MKK7在镉和亚砷酸钠激活D-JNK中的作用。方法细节:用RNAi分别敲减D-MKK4、D-MKK7的mRNA,或同时敲减两种基因,4天后用RT-PCR验证mRNA敲减效率,随后用200μM氯化镉或亚砷酸钠处理2h,检测磷酸化D-JNK水平。结果解读:图4A显示RNAi可将D-MKK4和D-MKK7的mRNA敲减至RT-PCR检测不到的水平;图4B和C的定量结果显示,敲减D-MKK7可使镉和亚砷酸钠诱导的D-JNK激活水平降低约70%(n=3,P<0.01,文献未明确提供具体数值,基于图表趋势推测),而敲减D-MKK4无明显抑制作用,同时敲减两种基因也未进一步增强抑制效果,说明D-MKK7是介导重金属激活D-JNK的主要JNKK。产品关联:实验所用关键产品:Invitrogen的Superscript反转录试剂盒、TA Cloning Kit,Ambion的MEGAscript T7转录试剂盒。
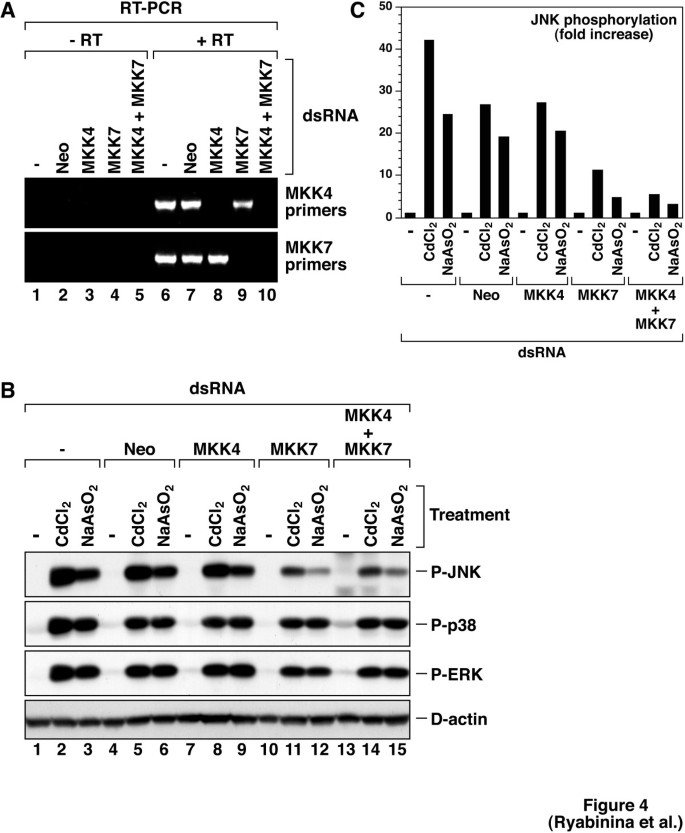
3.4 JNKKK在重金属激活D-JNK中的作用解析
实验目的:筛选介导镉和亚砷酸钠激活D-JNK的核心JNKKK。方法细节:用RNAi分别敲减D-ASK、D-MLK、D-MEKK1、D-TAK四种JNKKK的mRNA,或同时敲减四种基因,4天后用RT-PCR验证敲减效率,随后用200μM氯化镉、200μM亚砷酸钠、200mM白藜芦醇或50mM脂多糖(LPS)处理细胞,检测磷酸化MAP激酶水平。结果解读:图5显示敲减D-MEKK1可使镉和亚砷酸钠诱导的D-JNK激活水平降低约80%(n=3,P<0.01,文献未明确提供具体数值,基于图表趋势推测),而敲减D-ASK、D-MLK、D-TAK无明显抑制作用;同时敲减四种JNKKK可进一步增强抑制效果,但对LPS、白藜芦醇诱导的D-JNK激活无影响,说明D-MEKK1是介导重金属激活D-JNK的核心JNKKK,其他JNKKK仅发挥次要作用;此外,敲减JNKKK对镉和亚砷酸钠诱导的D-ERK激活无影响,对D-p38的影响因重金属而异(镉诱导的D-p38激活可被同时敲减抑制,亚砷酸钠诱导的则不受影响)。产品关联:实验所用关键产品:Sigma-Aldrich的白藜芦醇、脂多糖(LPS)。
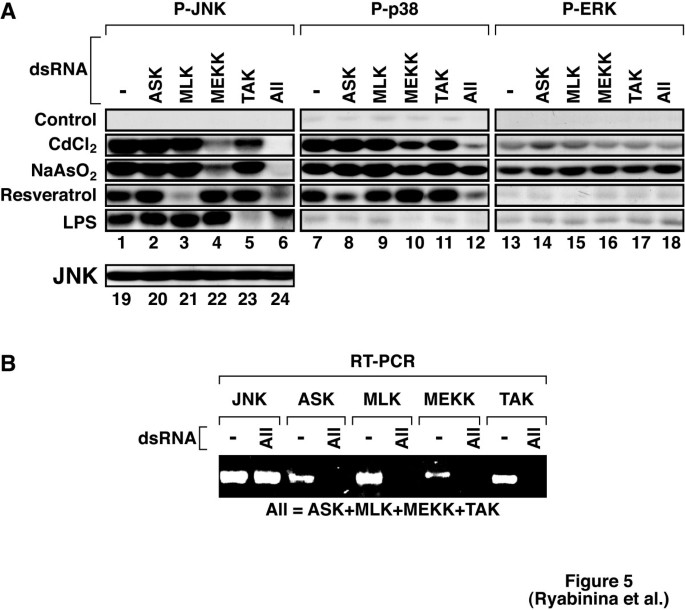
3.5 小G蛋白在重金属激活D-JNK中的作用解析
实验目的:验证小G蛋白是否参与镉和亚砷酸钠激活D-JNK的信号通路。方法细节:用RNAi同时敲减D-Rho1、D-RhoL、D-RalA、D-Rac1、D-Rac2、D-cdc42、D-Ras七种小G蛋白的mRNA,4天后用RT-PCR验证mRNA敲减效率,用蛋白免疫印迹验证D-Ras蛋白的敲减效果,随后用重金属处理细胞,检测磷酸化MAP激酶水平。结果解读:图6显示RNAi可将七种小G蛋白的mRNA敲减至检测不到的水平,且D-Ras蛋白水平显著降低;但重金属诱导的三种MAP激酶激活水平未受影响,说明这些小G蛋白不参与重金属激活D-JNK的通路,这与D-MEKK1缺乏小G蛋白结合基序的结构特征一致。产品关联:实验所用关键产品:Calbiochem的Ras抗体。
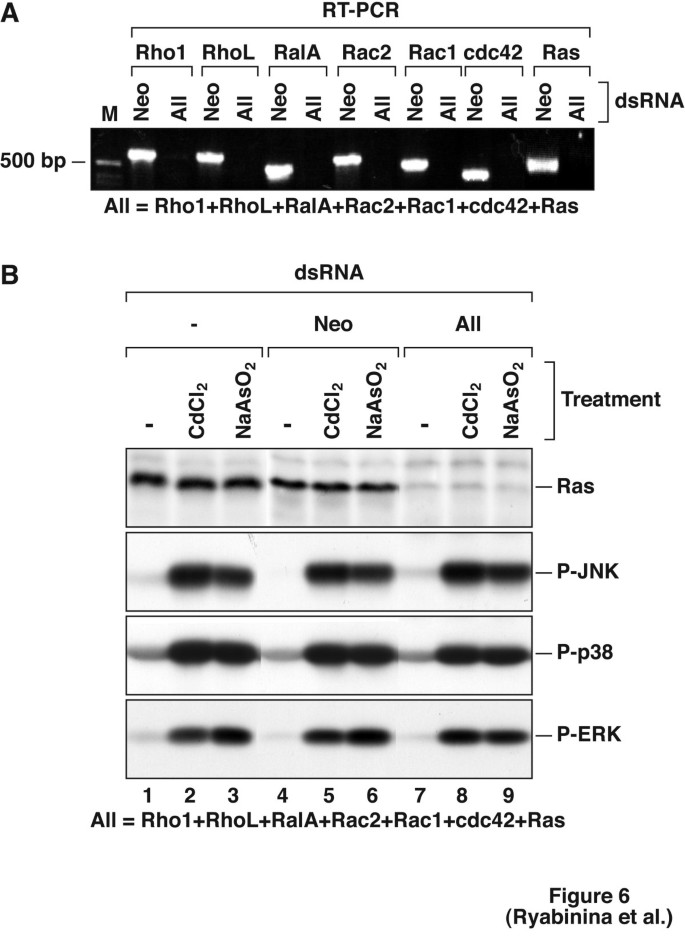
3.6 MEKK家族的进化保守性分析
实验目的:明确D-MEKK1与哺乳动物MEKK家族成员的进化关系,为信号模块的保守性提供依据。方法细节:对果蝇、人、小鼠的MEKK家族成员进行多序列比对,用Clustal X、Phylip和TreeView软件构建进化树,分析激酶结构域与N端调控域的保守性。结果解读:图7显示D-MEKK1与人MEKK4/MTK1、小鼠MEKK4的同源性最高,激酶结构域的氨基酸一致性达53%,N端调控域存在部分保守基序(如富含脯氨酸基序、PH结构域),但缺乏哺乳动物MEKK1和MEKK4的小G蛋白结合基序,这与之前的功能实验结果一致,说明小G蛋白调控可能是哺乳动物MEKK家族进化出的新功能,而重金属诱导的MEKK-JNK激活模块具有古老的进化起源。产品关联:文献未提及具体实验产品,领域常规使用Clustal X、Phylip、TreeView等生物信息学分析软件。
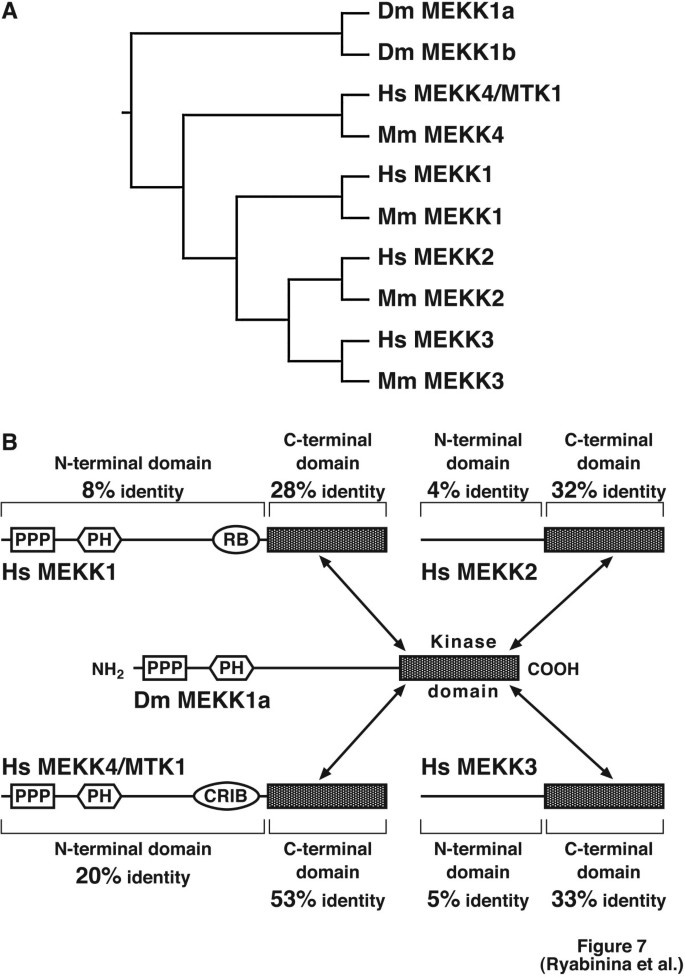
4. Biomarker研究及发现成果解析
文献中核心发现的Biomarker为信号通路关键调控激酶D-MEKK1和D-MKK7,属于功能型Biomarker,可作为重金属诱导细胞应激反应的核心调控靶点,其筛选与验证基于果蝇S2细胞的简化系统与进化保守性分析。
D-MEKK1(哺乳动物MEKK4/MTK1的同源物)和D-MKK7是镉和亚砷酸钠激活D-JNK的必需上游激酶,筛选逻辑为“果蝇模型简化→RNAi高通量敲减→功能验证→进化保守性确认”:先利用果蝇系统的基因冗余度低的优势,缩小候选因子范围;再通过RNAi敲减结合免疫印迹验证每个因子对D-JNK激活的影响;最后通过进化分析确认其与哺乳动物同源物的保守性,为哺乳动物相关研究提供参考。
Biomarker来源为果蝇S2细胞的内源性激酶,验证方法包括:1)RNAi敲减后用RT-PCR检测目标mRNA水平,确认敲减效率;2)蛋白免疫印迹检测磷酸化D-JNK水平,验证激酶对D-JNK激活的调控作用;3)进化分析确认其与哺乳动物同源物的保守性。特异性数据显示,敲减D-MEKK1仅抑制镉和亚砷酸钠诱导的D-JNK激活,对LPS、白藜芦醇诱导的激活无影响;敲减D-MKK7同样特异性抑制重金属诱导的D-JNK激活。敏感性方面,RNAi可将目标mRNA敲减至RT-PCR检测不到的水平,且蛋白水平(如D-Ras)显著降低,确保了功能验证的可靠性。
D-MEKK1和D-MKK7构成了进化保守的重金属诱导JNK激活的核心信号模块,其功能在果蝇与哺乳动物系统中具有保守性;创新性在于首次在简化模型中明确了该核心模块,解决了哺乳动物系统因冗余导致的研究矛盾;统计学结果显示实验重复3次(n=3),敲减D-MEKK1和D-MKK7后D-JNK激活水平显著降低(P<0.01,文献未明确提供具体数值,基于图表趋势推测);该发现为重金属诱导的细胞应激反应机制研究提供了新的靶点,同时为利用果蝇模型研究人类相关疾病的信号通路提供了依据。
